背景
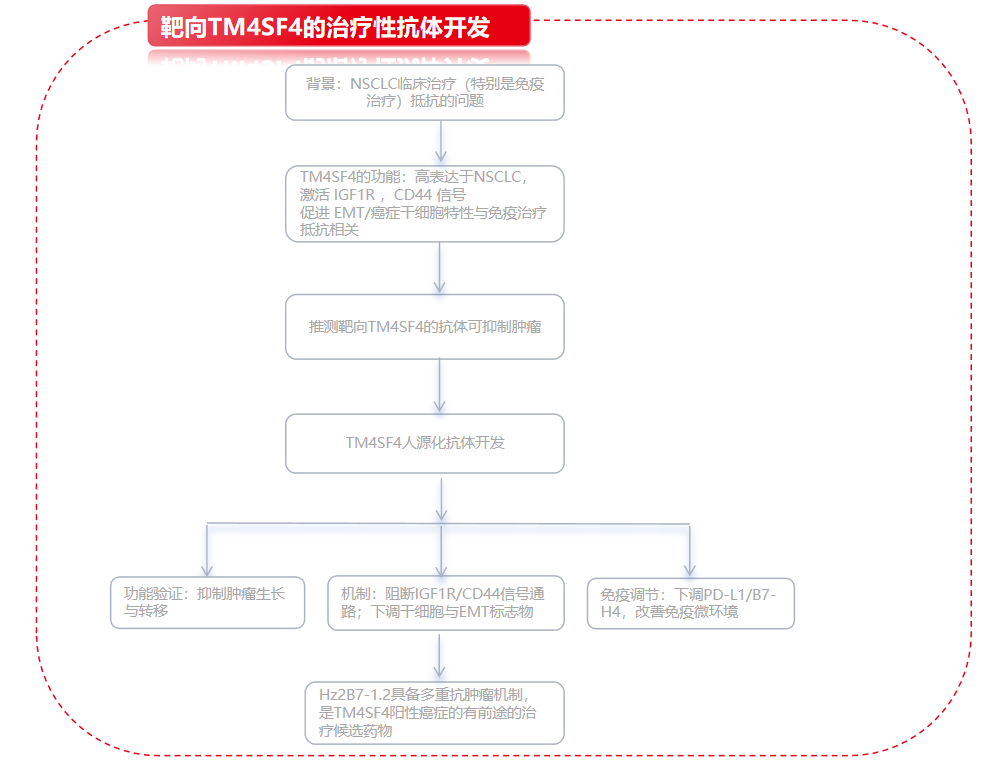
跨膜4超家族成员4(TM4SF4)已被证实是非小细胞肺癌(NSCLC)细胞中与上皮-间质转化(EMT)相关的干细胞特性密切相关的关键调节因子,其作用机制涉及胰岛素样生长因子1(IGF1)和骨桥蛋白(OPN)的自分泌信号传导。鉴于其在肿瘤进展和治疗抵抗中的关键作用,TM4SF4成为一个极具前景的治疗靶点。

韩国生物科学与生物技术研究所Eun-Wie Cho团队在Theranostics上发表了一篇名为“A novel TM4SF4-targeting therapeutic antibody candidate with antitumor activity by blocking IGF1R and CD44 signaling and downregulating PD-L1 and B7-H4”的研究成果。该研究开发一种靶向TM4SF4的治疗性抗体,人源化抗TM4SF4抗体Hz2B7-1.2通过多种机制表现出强大的抗肿瘤活性,包括抑制致癌信号通路、减少EMT相关干性和调节免疫反应。这些发现支持Hz2B7-1.2作为TM4SF4阳性癌症的有前途的治疗候选药物,值得进一步的临床研究。
抗hTM4SF4单克隆抗体的制备
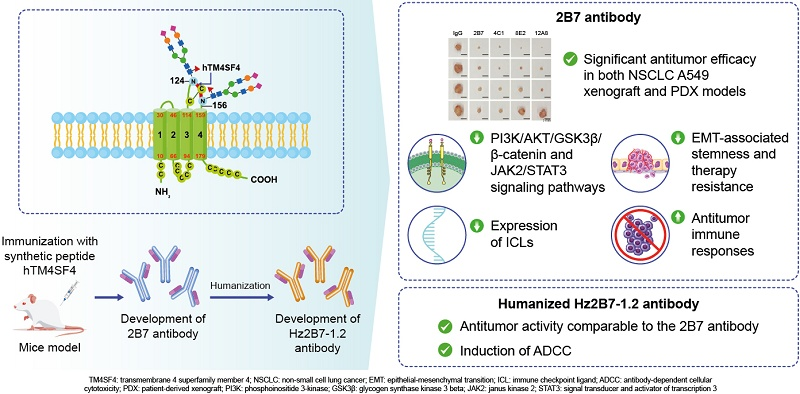
使用Kolaskar和Tongaonkar方法分析TM4SF4蛋白序列,最后发现T126-E140序列作为最佳表位。它位于C120-C146环的中心,包含预测的抗原位点(W127-D133),同时避开N124处的糖基化位点。合成15聚体肽hTM4SF4(T126-E140),并使用SMCC交联剂与BSA偶联,免疫小鼠在小鼠中产生抗TM4SF4单克隆抗体,免疫荧光发现新型抗体特异性识别细胞膜上TM4SF4的胞外结构域。通过SPR分析测量抗hTM4SF4 mAb与hTM4SF4肽的结合亲和力。2B7、4C1和12A这三种mAb都表现出纳摩尔级的结合亲和力,表明与表位肽有很强的相互作用,其中2B7表现出最高的结合亲和力。

2B7抗体在NSCLC异种移植模型中显示出有效的抗肿瘤功效,可抑制TM4SF4介导的癌症干性和EMT,并提供了其在肺外癌症类型中的治疗潜力的证据。

2B7治疗减少了IGF1Rβ磷酸化,降低了IL-1β、OPN和IGF1水平。这破坏了PI3K/AKT/GSK3β 和β-连环蛋白信号传导。OPN减少还会减少CD44激活,通过JAK2/STAT3和FAK/STAT3途径损害EMT相关的癌症干性。 2B7通过抑制关键癌症干细胞和EMT途径作为NSCLC治疗抗体的潜力。2B7不仅作为单独的抗肿瘤药物有效,而且与放疗或靶向治疗联合使用时,还可以通过抑制CSC特性和克服治疗耐药性来增强治疗效果。TM4SF4信号传导可促进免疫检查点配体(ICL) 表达,从而促进免疫逃避。2B7不仅抑制癌细胞中的ICL表达,而且还降低了外泌体ICL水平,可能增强抗肿瘤免疫反应。

人源化2B7抗体的构建和表征
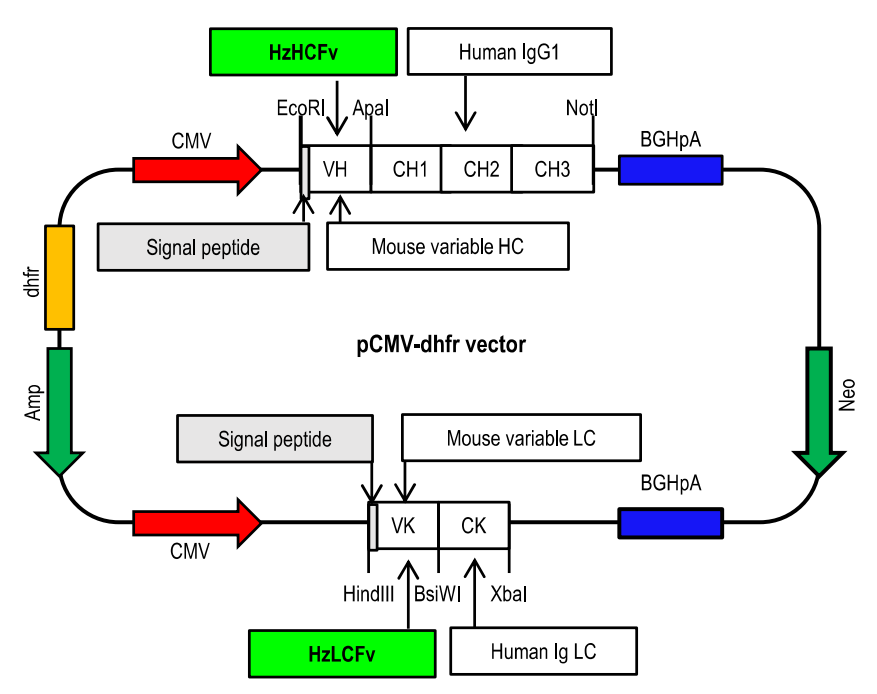
将鼠源2B7的可变区与人源IgG1恒定区(Fc)和κ轻链恒定区融合构建嵌合抗体(Chi2B7)。将2B7 CDR的基因,移植到人抗体3QRG的框架区上,该基因与2B7 VH和Vκ区表现出最高的序列同源性。将所得人源化2B7 VH(Hz2B7-1.0)和Vκ(Hz2B7-0.1)基因亚克隆到pdCMV-dhfr 载体中,生成Hz2B7-1.1表达构建体。基于分子对接模拟(使用AutoDock)分析抗原-抗体结合界面,通过CDR或FR残基中引入靶向突变,对Hz2B7-1.1抗体进行亲和力成熟。Hz2B7-1.2(VκN31F)表现出最优结合亲和力,被选为主导候选抗体。
Hz2B7-1.1结合活性在96小时内保持稳定,与生产细胞系(HEK293T或CHO)无关。观察到Hz2B7-1.1和鼠2B7抗体具有相当的稳定性,表明Hz2B7-1.2在人血清中结构稳定。

Hz2B7-1.2表现出抗癌作用并介导针对表达TM4SF4的癌细胞的细胞毒性
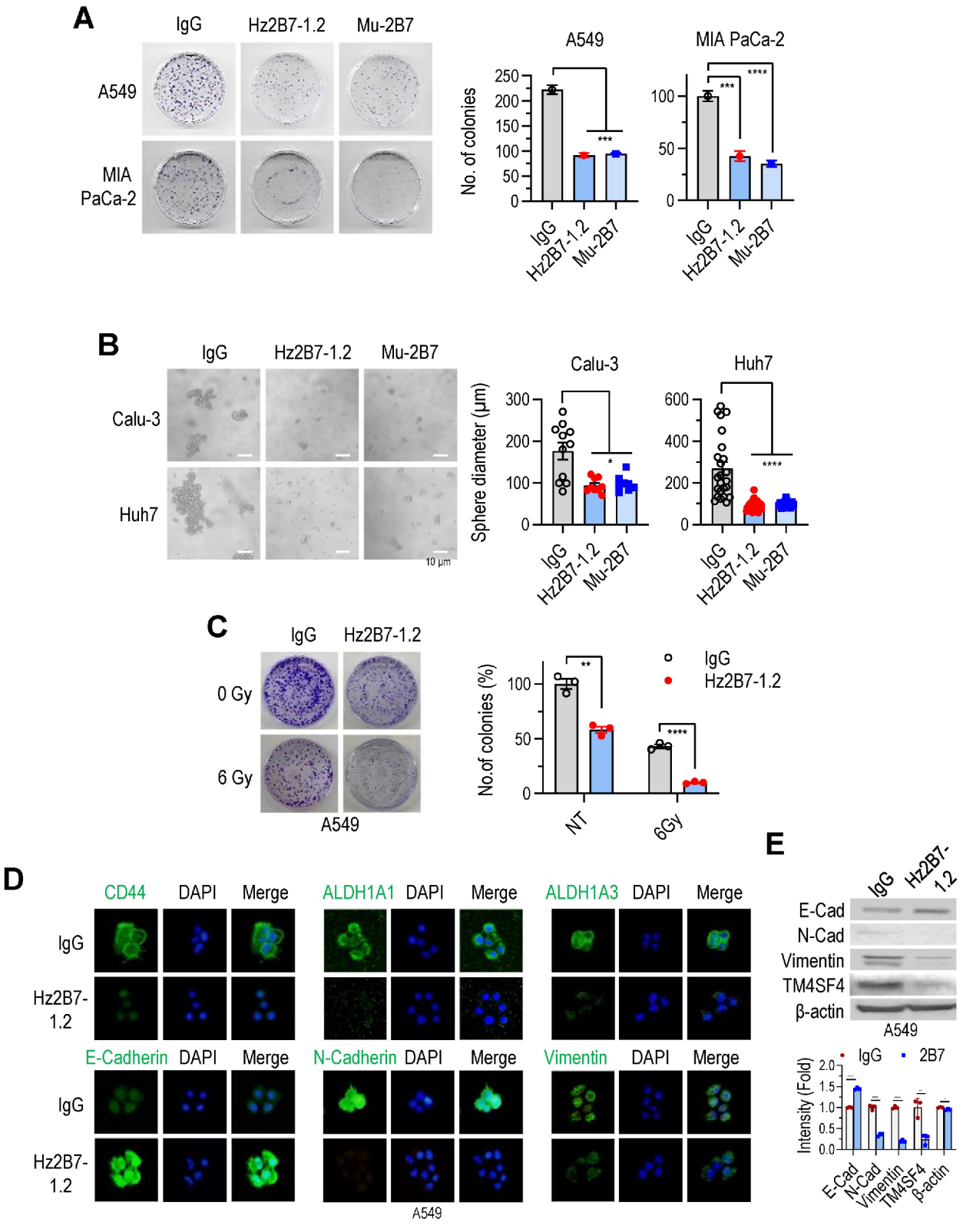
人源化2B7抗体Hz2B7-1.2抑制癌细胞生长和自我更新,Hz2B7-1.2在同等剂量下表现出比嵌合Chi2B7抗体更高的ADCC活性,这可能是由于TM4SF4结合增强。人源化Hz2B7-1.2抗体成功移植并保留了亲本鼠2B7抗体的优异TM4SF4靶点结合特性。此外,作为IgG1同种型,Hz2B7-1.2可有效介导针对表达TM4SF4的癌细胞的抗体依赖性细胞毒性 (ADCC),从而清除肿瘤。其在肿瘤小鼠模型中的抗肿瘤功效明显低于鼠2B7抗体,这种功效降低可能是由于鼠类和人源化抗体之间的结构和功能差异,特别是IgG1型人源化抗体中引入的效应细胞募集功能,而鼠类IgG1抗体中不存在这种功能。

总结
本研究开发了一种针对人TM4SF4的鼠单克隆抗体(抗hTM4SF4 mAb),命名为2B7,它在NSCLC 中表现出有效的抗癌作用。体外和体内实验证明2B7的抗癌功效是通过抑制IGF1/IGF1Rβ和 OPN/CD44信号传导以及通过下调PD-L1和B7-H4抑制免疫逃避来介导的。通过CDR移植和亲和力成熟生成了人源化版本,并评估了其作为抗癌药物的治疗潜力,它可以抑制癌细胞生长和自我更新介导针对表达TM4SF4的癌细胞的细胞毒性。体内实验显示,Hz2B7-1.2在全身给药后的抗肿瘤效果较鼠源2B7有所下降,这一差异可能与Fc段介导的免疫细胞相互作用变化有关。
为提升Hz2B7-1.2的疗效,下一步优化将聚焦于保留Fab介导的靶标结合、减少FcγR结合以维持较高的游离抗体水平,并保留FcRn亲和力以实现最佳血清稳定性。潜在的策略包括Fc聚糖修饰或将亚类转换为IgG2 或IgG4,最大限度地减少免疫细胞相互作用。未来的研究将集中于Hz2B7-1.2的此类优化,以最大限度地发挥其临床潜力。鉴于2B7在肝细胞癌和胰腺癌模型中已证明有效,抗TM4SF4单克隆抗体疗法可能广泛适用于其他TM4SF4过表达的肿瘤,支持通用CSC靶向癌症疗法的开发。
