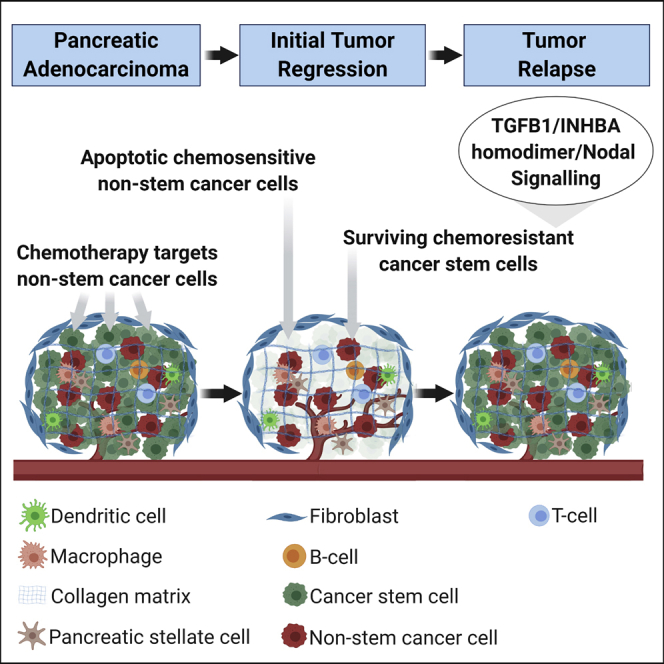
抑制素/活化素参与调节多种不同的功能,如下丘脑和垂体激素分泌、性腺激素分泌、生殖细胞发育和成熟、红细胞分化、胰岛素分泌、神经细胞存活、胚胎轴向发育或骨生长,这取决于它们的亚基组成。抑制素βA(INHBA)属于转化生长因子-β (TGF-β) 超家族,该超家族分为两个主要功能组:转化生长因子β样组,包括转化生长因子β的不同亚型(TGFB1、TGFB2和TGFB3)、INHBA、抑制素β B亚基(INHBB)、抑制素βC亚基(INHBC)、抑制素β E亚基(INHBE)、抑制素α亚基(INHA)、Nodal和一些生长分化因子;以及骨形态发生蛋白样组,包括骨形态发生蛋白、抗苗勒管激素(AMH)和大多数生长分化因子。INHBA参与形成活化素或抑制素,INHBA的同源二聚体活化素A(Activin A)在调节免疫反应和肿瘤进展方面具有多效性,包括胚胎发育、干细胞维持和分化、造血、细胞增殖和组织纤维化。
(数据来源 Abdel Mouti M, et al. Mol Ther. 2021)
INHBA的表达分布
INHBA主要表达在成纤维细胞、滋养细胞、间质细胞、中性粒细胞中,INHBA在睾丸的发育和功能中起着至关重要的作用,并调节卵巢组织和卵母细胞的生长。
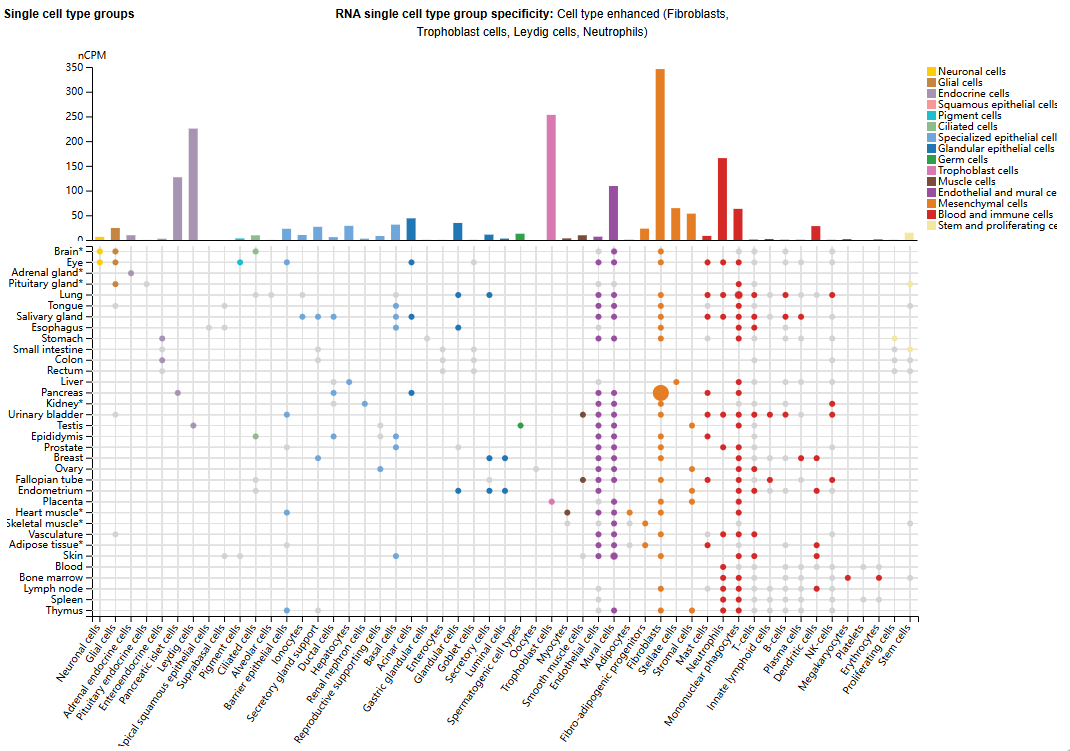
(数据来源 uniprot)
INHBA的表达水平在多种癌症类型中升高,包括乳腺癌(BRCA)和结肠腺癌(CRC)。此外,生存分析也证实,INHBA的表达与许多癌症患者的预后呈负相关。
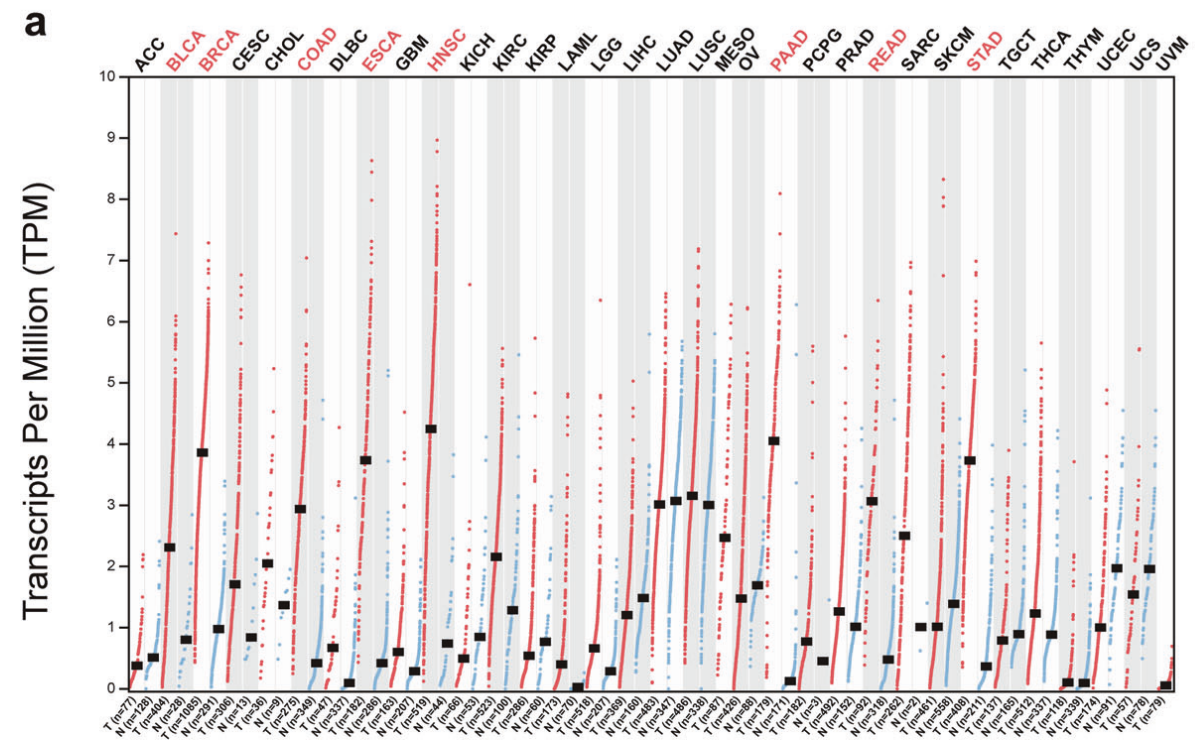
(数据来源Li FL, et al. Acta Pharmacol Sin. 2025)
INHBA的结构
INHBA是一种分泌蛋白,由426个氨基酸组成,成熟的INHBA蛋白包含一个高度保守的TGF-β样结构域,该结构域是TGF-β超家族成员的标志性功能区域,负责介导配体与其受体的特异性结合以及随后的信号转导。INHBA蛋白一般以同源二聚体(即激活素A)或异源二聚体(如激活素AB)的形式存在。
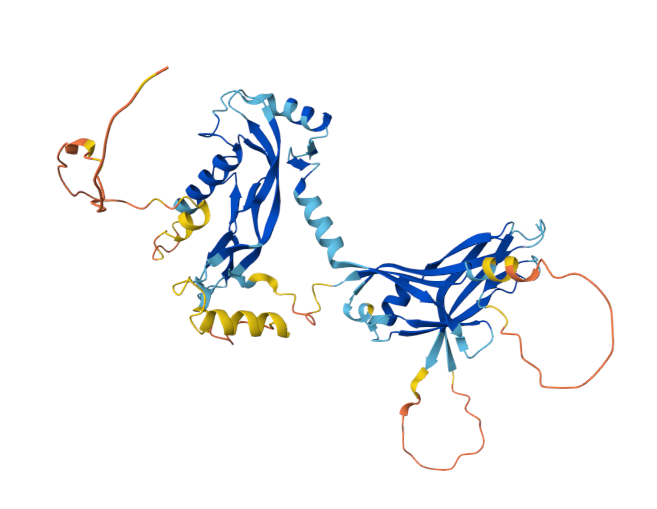
(数据来源 Alphafold)
INHBA的信号转导和在癌症中的作用机制
TGFB1、INHBA同二聚体和Nodal属于转化生长因子超家族的细胞因子,TGFB1/INHBA同二聚体/Nodal信号的经典途径是依赖SMAD的。TGFβ1、INHBA二聚体以及Nodal蛋白与各自跨膜型II受体(TGFBR2对于TGFβ1,ACVR2A/ACVR2B对于INHBA二聚体/Nodal)的细胞外结构域相结合,从而将I型跨膜受体(TGFBR1对于TGFβ1,ACVR1B对于INHBA二聚体/Nodal)招募至配体-受体复合物中,通过其GS结构域内的多个丝氨酸和苏氨酸残基的磷酸化实现受体的激活。ZFYVE9调节SMAD2/3对激活受体复合物的进入,其中SMAD2/3与激活型I型受体之间的相互作用通过磷酸化的GS结构域、L45环以及SMAD2/3的L3环介导,导致SMAD2/3磷酸化,随后与ZFYVE9解离并结合到SMAD4上。活性的SMAD2/3/4转录复合物随后转移到细胞核中,在与DNA结合转录因子和核心调节因子结合的同时,与特定的SBE序列结合,从而控制靶基因的表达。
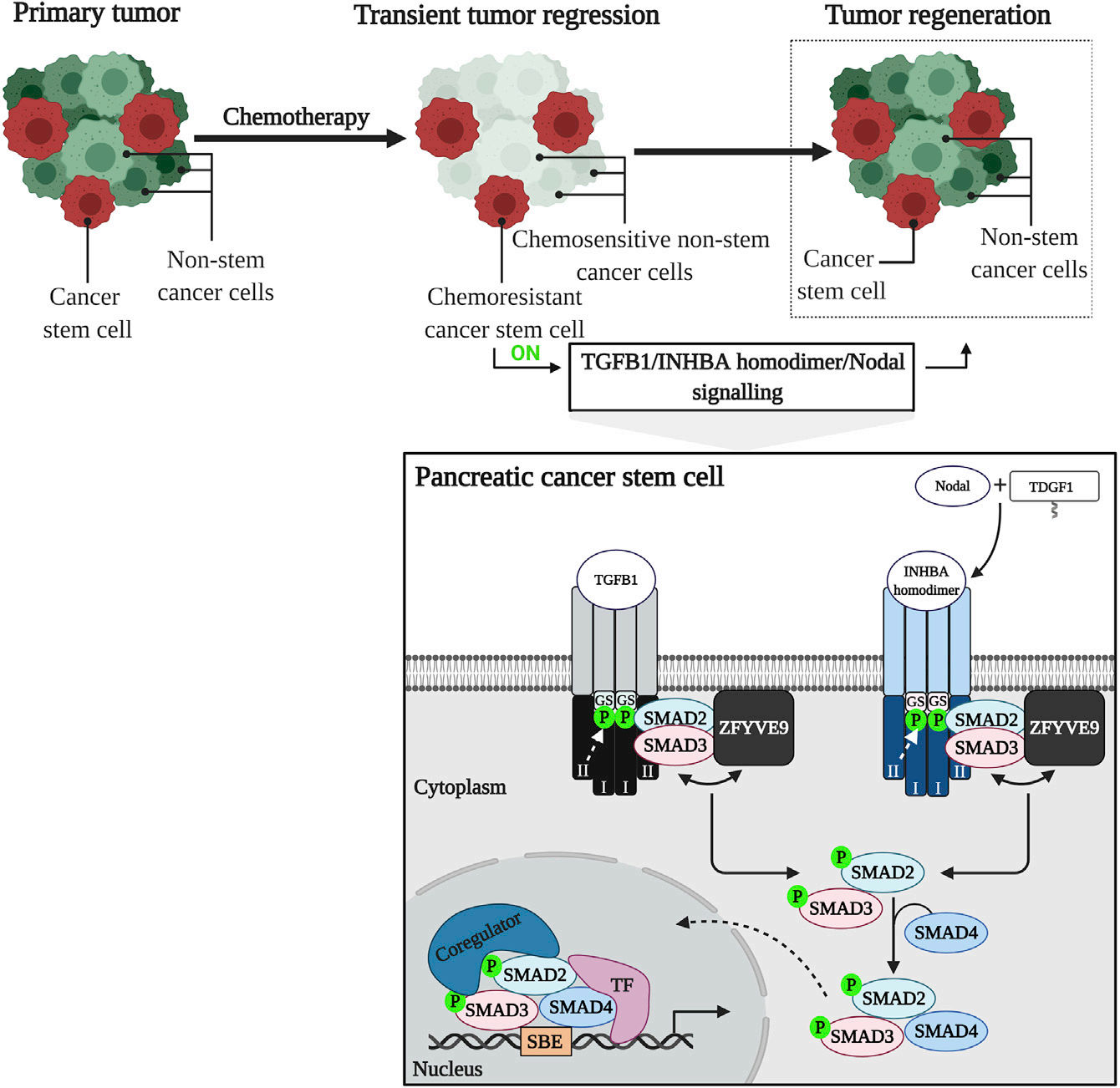
(数据来源 Abdel Mouti M, et al. Mol Ther. 2021)
胰腺导管腺癌微环境中的基质成分通过TGFB1/INHBA同聚体/Nodal增强PCSCs的干细胞样特征、肿瘤发生能力以及化疗耐药性。肿瘤相关巨噬细胞(TAMs)分泌的TGFB1以及PSCs(肿瘤干细胞)分泌的INHBA二聚体/Nodal通过激活PCSCs中的TGFB1/INHBA二聚体/Nodal信号通路,从而维持其干细胞样特性,并增强其肿瘤发生能力以及对化疗的抵抗性,导致肿瘤复发和治疗失败。PSCs中的TGFB1-SMAD3信号通路还通过调节I型胶原蛋白在细胞外基质中的合成和沉积,从而促进化疗耐药性,导致广泛的纤维化,这会妨碍有效将治疗药物递送至肿瘤内部。在受到由PCSCs分泌的INHBA二聚体/Nodal激活后,TAMs分泌LL-37/hCAP-18肽,这会驱动PCSCs的自我更新并促进其肿瘤发生能力。
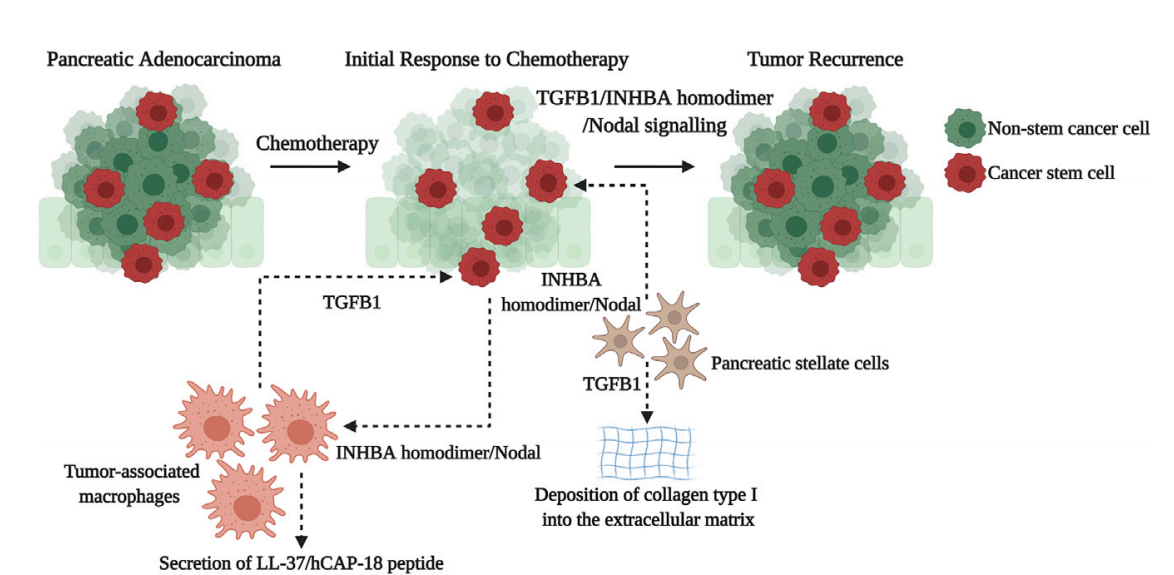
(数据来源 Abdel Mouti M, et al. Mol Ther. 2021)
作为TGF-β信号的关键配体,INHBA可以激活TGF-β通路,启动磷脂酰肌醇-3-激酶/蛋白激酶B(PI3K/Akt)通路,增加细胞周期蛋白D1的表达,并加速细胞周期进程,从而驱动CRC细胞增殖。此外,沉默INHBA基因可以通过抑制TGF-β信号通路,抑制胃癌细胞和骨肉瘤细胞的增殖、迁移和侵袭。
研究发现INHBA、SLC25A10和TRIM21是相互作用的蛋白质。INHBA作为一种支架蛋白,通过K48连接的泛素化阻止TRIM21降解SLC25A10,从而提高其稳定性。此外,INHBA通过增强SLC25A10蛋白水平来促进succinate/SUCNR1通路,诱导M2巨噬细胞极化。它还激活了mtGSH/GPX4轴,从而抑制线粒体依赖的铁死亡。这些改变最终促进了结直肠癌的侵袭性生长。
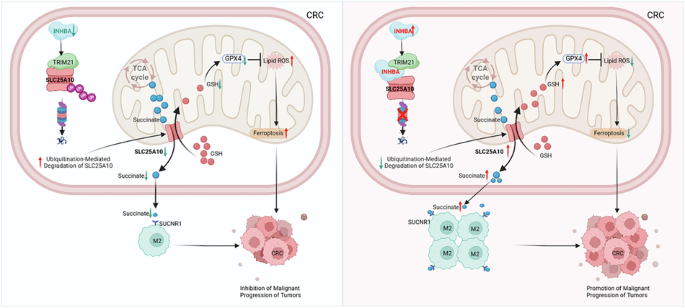
(数据来源 Li W, et al. Signal Transduct Target Ther. 2025)
INHBA的靶向治疗
由于INHBA在各种肿瘤中的上调及其在肿瘤进展中的重要作用,它成为了一个肿瘤治疗靶点,许多针对INHBA的抗体在临床开发中。
Garetosmab是再生元制药开发的一款靶向INHBA的单克隆抗体用于治疗罕见病,可阻断Activin A。Activin A在FOP患者异位骨化(HO)病变的发展中起着关键作用。是唯一一种被证明能显著减少FOP患者异常骨病变(异位骨化,或HO病变)数量和体积的治疗方法。2025年临床3期实验主要终点已达成,在56周时新HO病变减少90%或以上,并且Garetosmab还导致新HO病变总体体积减少99%以上。2026年2月19日,再生元宣布美国食品和药物管理局(FDA)已经接受了用于治疗成人进行性FOP的Garetosmab生物制品许可申请(BLA)的优先审查。
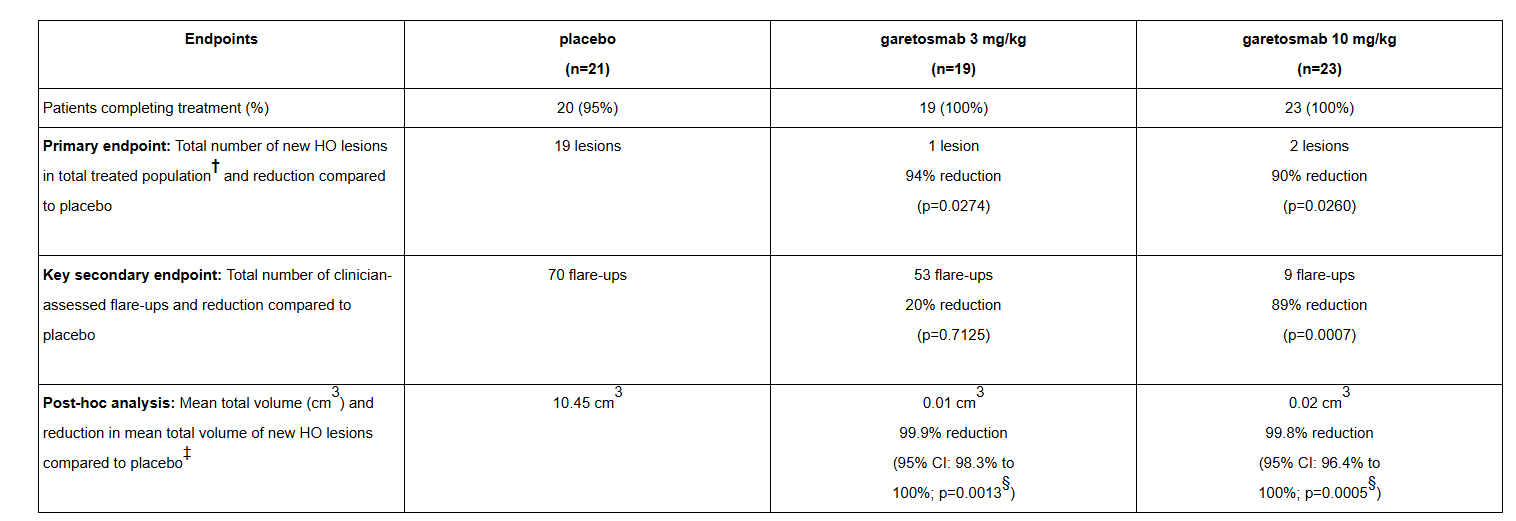
(数据来源 再生元制药官网)
Sotatercept是默沙东公司(美国新泽西州拉威)开发的一种activin信号抑制剂,用于治疗肺动脉高压(PAH),于2024年3月26日在美国获得首次批准。Sotatercept是一种同二聚体重组融合蛋白,由人类激活素受体IIA类型的胞外结构域与人类免疫球蛋白G1的Fc结构域连接而成。它通过与activin A(以及其他转化生长因子-β超家族配体)结合来抑制激活素信号传导,从而调节血管增生,通过促增殖和抗增殖信号通路(分别由ActRIIA/Smad2/3和BMPRII/Smad1/5/8介导)来实现这一作用。
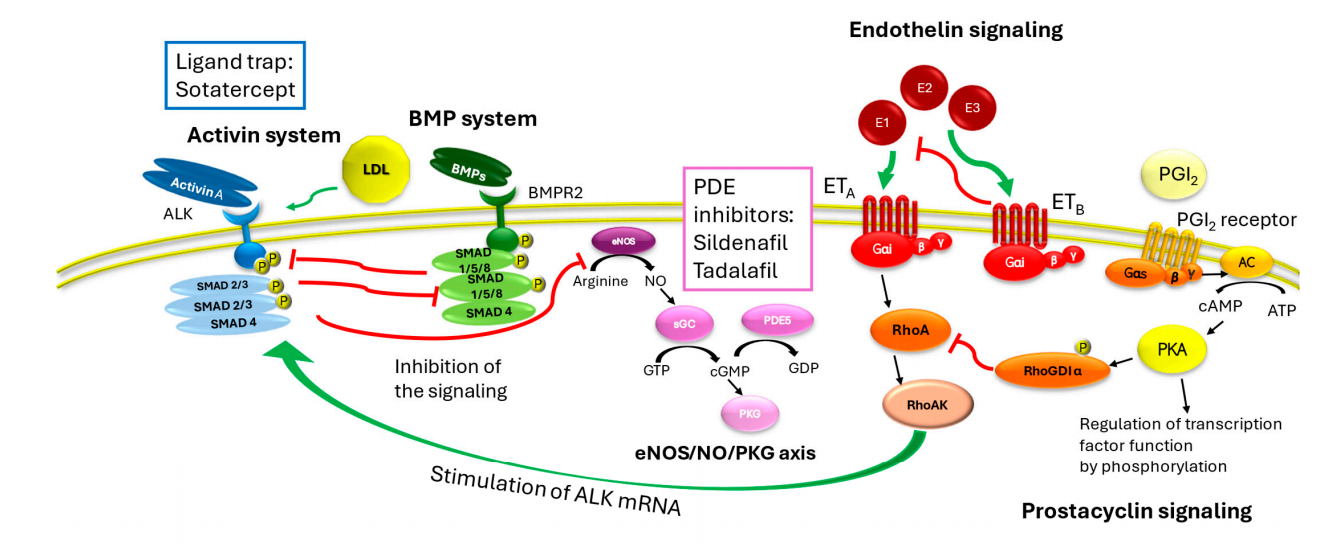
(数据来源 Madonna R, et al. Int J Mol Sci. 2025)
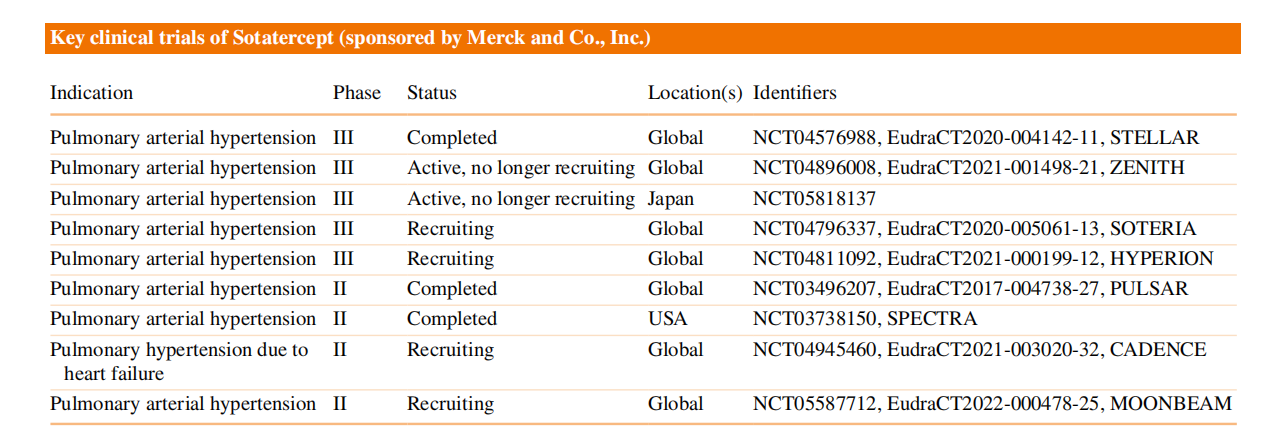
(数据来源 Kang C.Drugs. 2024)
我们收集整理一批INHBA相关抗体序列信息。文档可关注公众号“迈思生物”,号内回复“INHBA”下载。
