补体系统是先天免疫的重要组成部分,可以通过三种途径激活:经典途径(CP)、替代途径(AP)和凝集素途径(LP)。

(数据来源 Thomas D, et al. Front Immunol. 2023)
凝集素途径(LP)被发现的最晚,甘露糖结合凝集素(MBL)、其他凝集素和聚脂素统称为LP的模式识别分子(PRMs),它们负责将LP激活为分子模式;另外MBL相关丝氨酸蛋白酶(MASP)是效应分子,而MBL相关蛋白(MAp)具有调节功能。当PRMs与靶表面结合时,相关的丝氨酸蛋白酶被激活,并通过切割和激活后续成分启动补体级联反应。由于一个活性蛋白酶可以切割和激活许多酶原分子,因此这种蛋白水解级联反应具有巨大的放大潜力。事实上,如果补体激活以不受控制的方式发生,它可能会导致严重疾病的发展和进展。

(数据来源 Daniel R, et al. Nat Rev Nephrol. 2016)
丝氨酸蛋白酶MASP
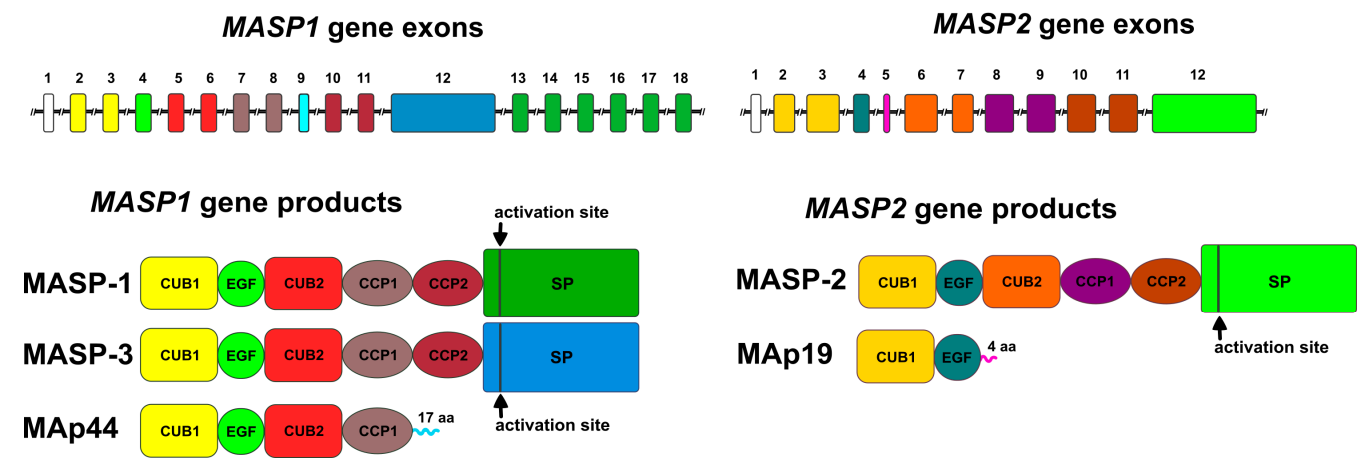
MBL相关丝氨酸蛋白酶(MASP)由MASP1及MASP2基因编码,通过选择性剪接或选择性多聚腺苷酸化形成不同产物蛋白,作为凝集素途径激活的效应分子,其成员中MASP1和MASP2负责触发凝集素途径的激活,而第三个成分MASP3参与补体系统替代途径(AP)的功能。
PRM/MASP1和PRM/MASP2复合物在活化表面聚集触发LP活化;PRM/MASP3复合物通过PCSK6裂解,随后由MASP3裂解pro-FD激活AP(红色箭头表示蛋白水解裂解,而蓝色箭头表示非酶促事件。棕色表示PRM,而灰色椭圆形表示激活面。)。
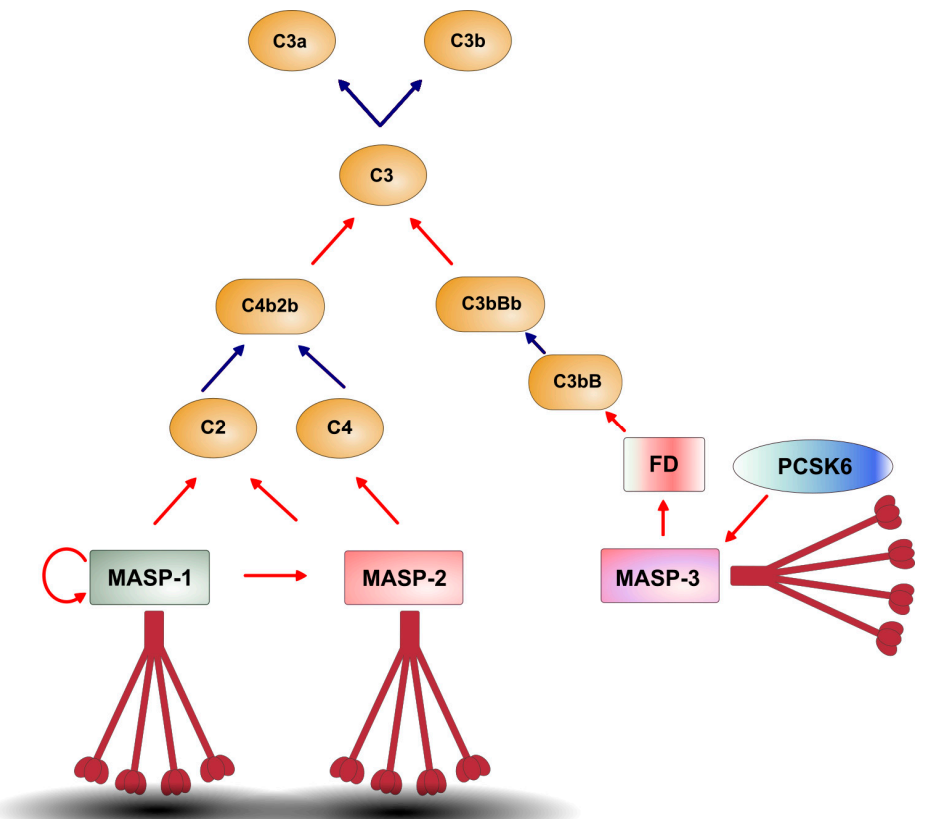
(数据来源 Dobó J, et al. Int J Mol Sci. 2024)
MASP结构
所有MASP蛋白都有相同的结构,即一个重/α链、一个轻/β链,以及一个连接的半胱氨酸二硫键。重链由两个CUB结构域和两个补体调节蛋白(CCP)结构域组成,由一个表皮生长因子段(EGF)连接。
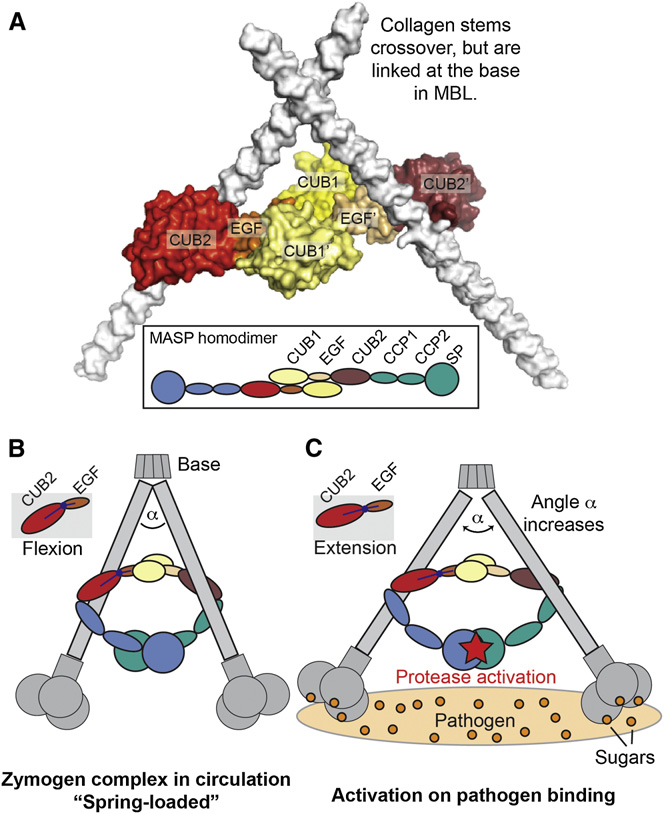
(数据来源 Alexandre R, et al. Structure. 2011)
MASP调控机制
当补体遇到免疫原时,识别分子C1q、甘露糖结合凝集素(MBL)、纤维蛋白原样蛋白(Ficolins)和收集素-11识别抗体簇或病原体相关分子模式(PAMPs),并激活相关的丝氨酸蛋白酶(MASPs),这些蛋白酶切割C4和C2以在触发细胞上形成经典途径(CP)和凝集素途径(LP)的C3转化酶(C4b2b),这些过程激活更多的C3生成C3b,并促进一个放大的循环。增加C3b浓度有利于C5转化酶的生成,这些酶激活C5以释放过敏毒素C5a和C5b,与C6-C9分步互动并插入膜后,形成膜攻击复合物(MACs),导致靶细胞的裂解、损伤或激活,释放出的过敏毒素作为免疫介质起作用,特别是在C5a的情况下,吸引并激活免疫细胞。

(数据来源 Daniel R, et al. Nat Rev Nephrol. 2016)
MASP的靶向治疗
目前围绕MASP靶点开发抑制剂的方向主要由两种:一种是针对MASP2(如Narsoplimab),虽然MASP1和MASP2都切割C2,但只有MASP2切割C4,允许形成C3转化酶C4b2a,另外抑制MASP-2似乎不会干扰经典补体途径,经典补体途径是感染后获得性免疫反应的重要组成部分,这种阻断药物被设计用于预防补体介导的炎症和内皮损伤,同时保持先天免疫其他途径的相应功能不受影响;另一种是针对MASP3(如Zaltenibart),因为MASP3是pro-FD转化为FD的唯一激活因子,是FD切割FB和形成替代途径(AP)C3转化酶C3bBb的关键调节因子,抑制MASP3在抑制补体激活、炎症和微血管停滞方面有潜在治疗效果。
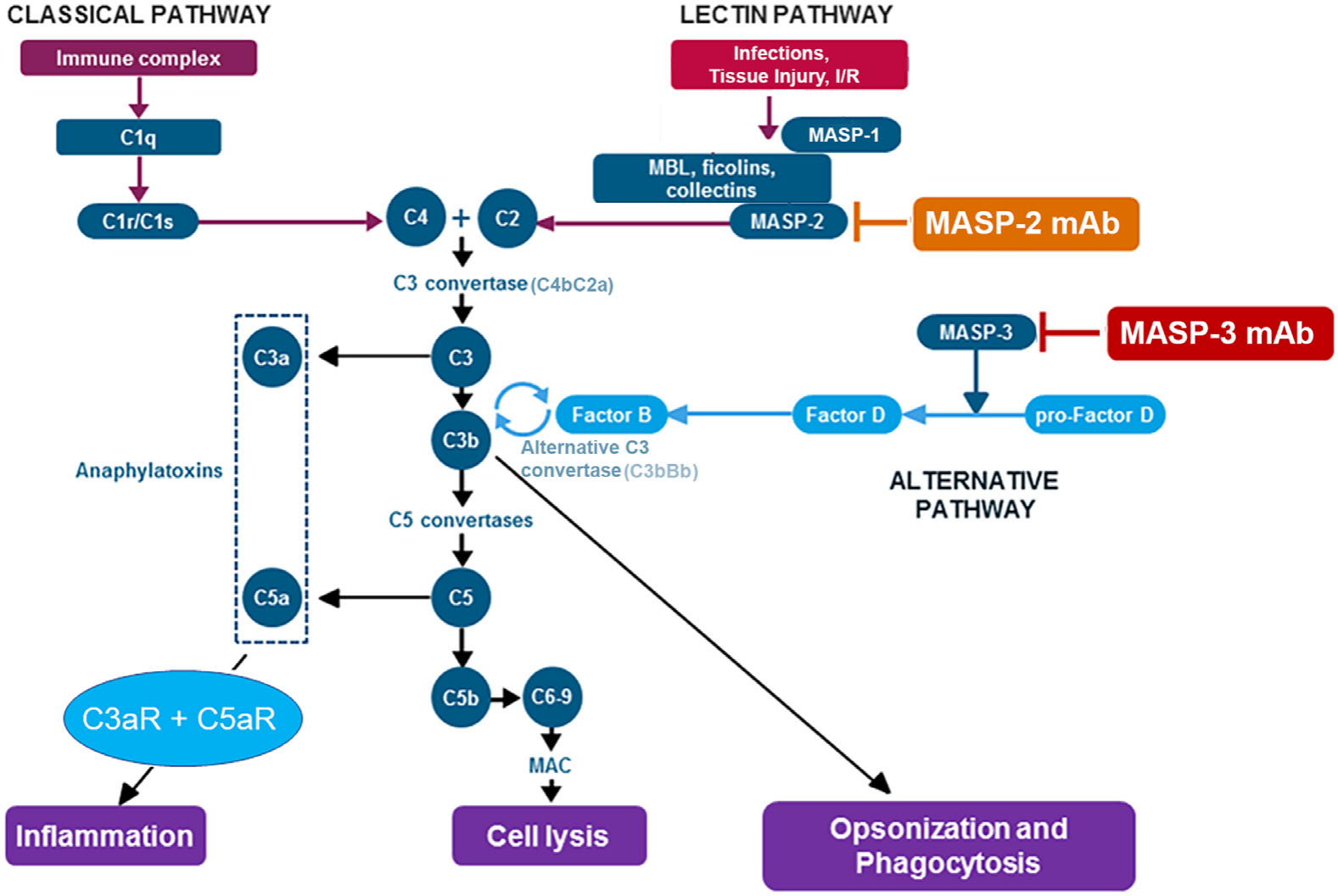
(数据来源 John D, et al. Transl Res. 2022)
有意思的是目前针对MASP开发靶向抗体治疗的公司主要是Omeros,管线上看该公司也是非常笃定MASP靶点的前景。

(数据来源 Omeros官网)
我们收集整理一批MASP相关抗体序列信息。文档可关注公众号“迈思生物”,号内回复“MASP”下载。
