人类白细胞抗原-G(HLA-G),这是一种非典型的主要组织相容性复合体(MHC)I类分子,HLA-G 通常在母体与胎儿的交界处以及某些免疫隔离区域表达。在癌症中,其表达被用作一种免疫逃逸策略。HLA-G通过与肿瘤浸润免疫细胞上的受体结合来发挥其强大的抑制作用。HLA-G通过ILT2 和ILT4(适应性免疫细胞亚群中的ILT2和固有免疫细胞亚群中的ILT2和ILT4)介导免疫抑制作用。阻断HLA-G有可能逆转免疫耐受并激活抗肿瘤免疫反应。

(数据来源 Tizonatx官网)
HLAG的表达分布
与经典的MHC I类分子不同,HLA-G的表达具有高度的特异性。在正常生理状态下,HLA-G仅存在于少数组织和细胞中,包括胎盘的绒毛外滋养层细胞、角膜和胸腺上皮细胞,通过与免疫细胞上的相应配体相互作用来实现免疫耐受。在多种病理条件下,如恶性肿瘤、病毒或微生物感染,以及自身免疫性疾病,HLA-G的表达会过度增加。HLA-G在一些肿瘤中含量较高,从而促进了免疫逃逸。
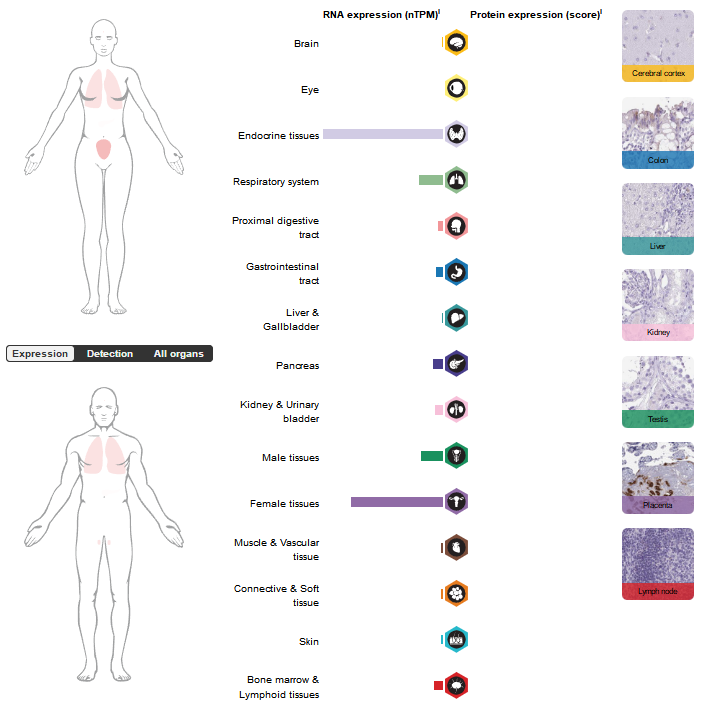

(数据来源 uniprot)
HLAG的结构和其受体
HLAG是一种单次跨膜I型膜蛋白,HLAG基因与经典的MHC分子高度同源,位于6p21.3染色体上,包含8个外显子,依次编码信号肽、细胞外的α1-α3结构域、跨膜结构域和细胞内区域。
HLAG通过选择性剪接产生7种不同的亚型,亚型HLA-G1、HLA-G2、HLA-G3和HLA-G4保留跨膜结构域以表达相应的膜结合蛋白,而HLA-G5、HLA-G6和HLA-G7因缺乏跨膜结构域而以可溶形式存在。
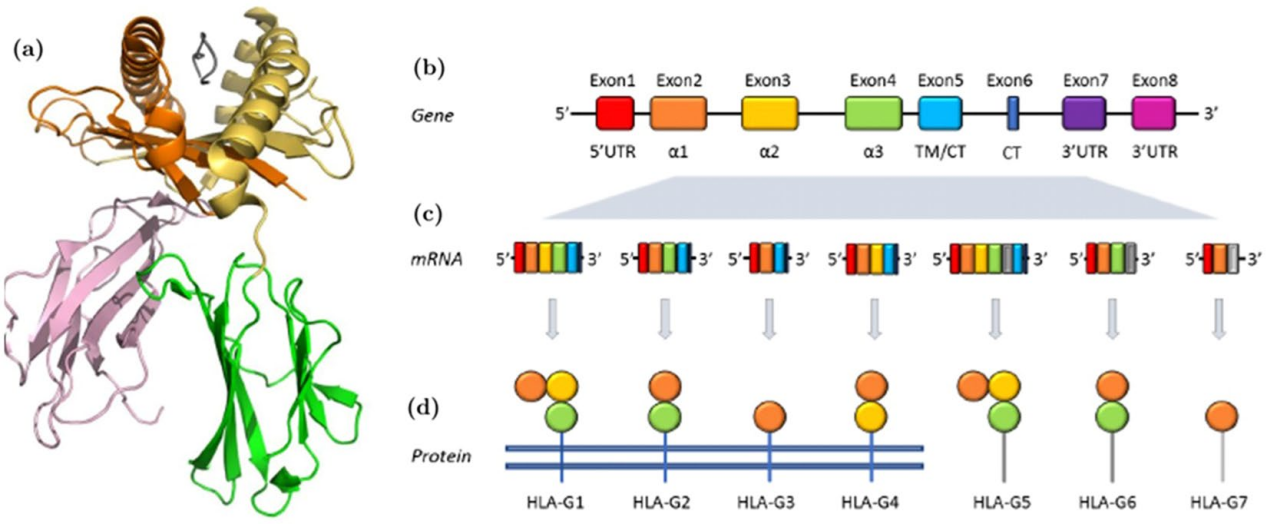
(数据来源 Scarabel L, et al. Sci Rep. 2020)

(数据来源 Wang S, et al. J Transl Med. 2024)
HLAG在肿瘤微环境中的作用
HLA-G能够抑制T细胞的细胞毒性及趋化性,并通过直接结合促进CD4+T细胞向Treg细胞的分化;而sHLA-G则能够驱动Th2细胞极化,并增强TIM-3的表达,从而间接对T细胞发挥抑制作用。同样地,HLA-G可以抑制NK细胞的细胞毒性、趋化性和迁移,同时诱导其凋亡和衰老。HLA-G还会抑制NK细胞的细胞毒性、趋化性和迁移,诱导B细胞的凋亡和衰老,并促使巨噬细胞极化向M2型转变。MDSC的增殖和积累受HLA-G的抑制。HLA-G也会抑制DC的激活和抗原呈递功能,并促进耐受性DC的诱导。需要注意的是,肿瘤细胞可以将HLA-G转移到其他肿瘤细胞和效应免疫细胞上,从而迅速导致免疫抑制的扩散。
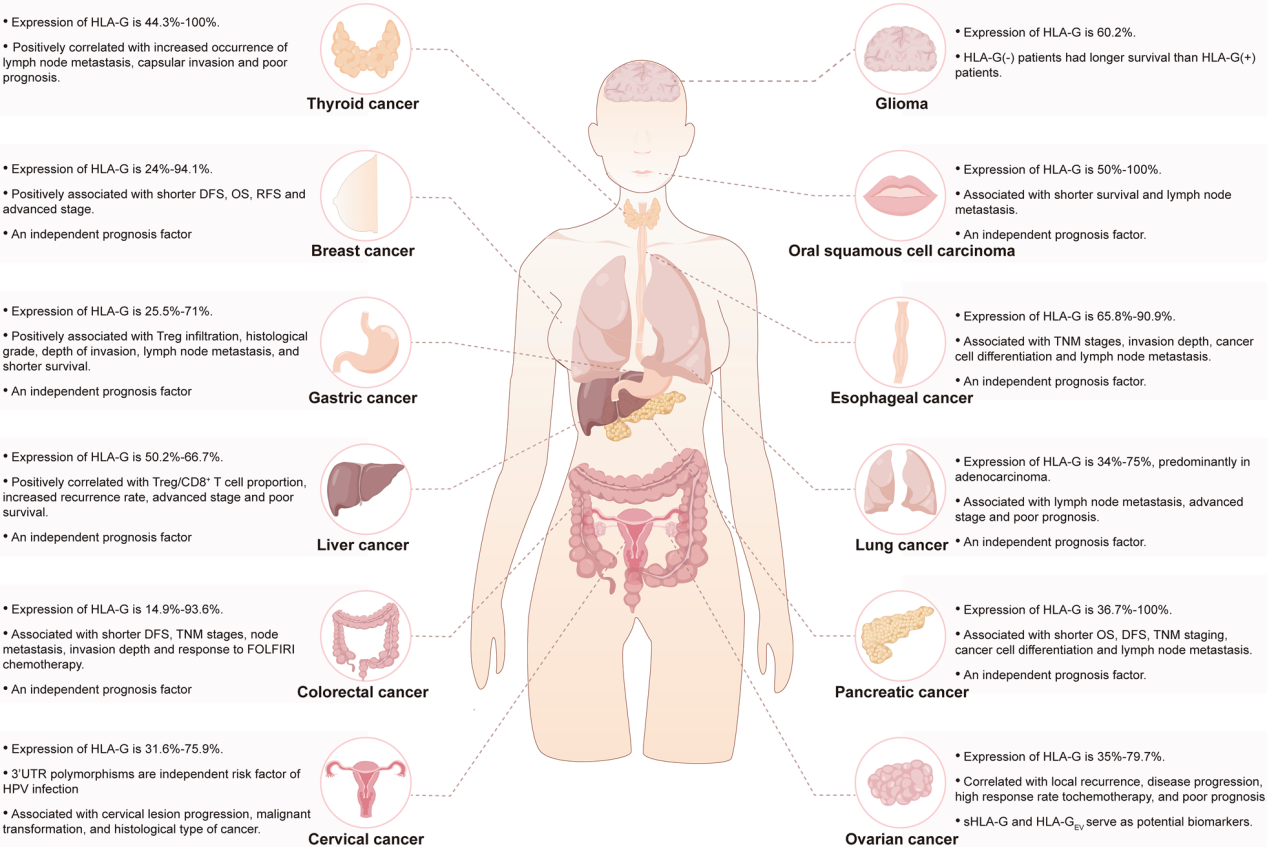
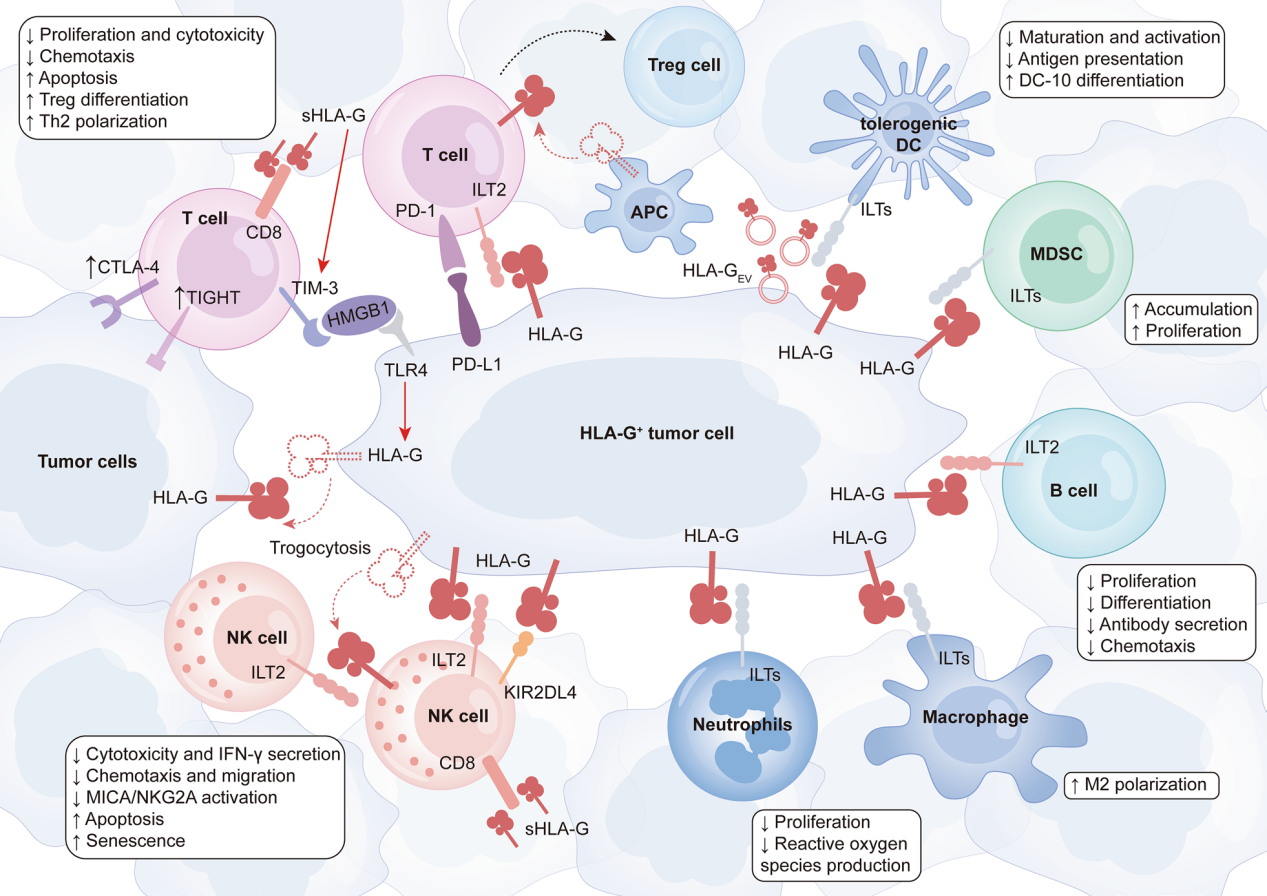
(数据来源 Wang S, et al. J Transl Med. 2024)
HLAG的靶向治疗
由于HLAG在肿瘤免疫中的作用,许多靶向HLAG的疗法在临床开发和临床研究阶段。针对HLA-G的单克隆抗体和CAR-NK细胞能够抑制肿瘤生长。抗HLA-G抗体也可作为化疗、免疫检查点阻断(ICB)、靶向治疗(包括CDK抑制剂、ERK抑制剂、AKT抑制剂和血管生成抑制剂)的良好搭档。此外,小分子抑制剂、miRNA模拟物和PROTAC(蛋白降解靶向偶联物)可能为HLA-G的未来应用提供新的机会。
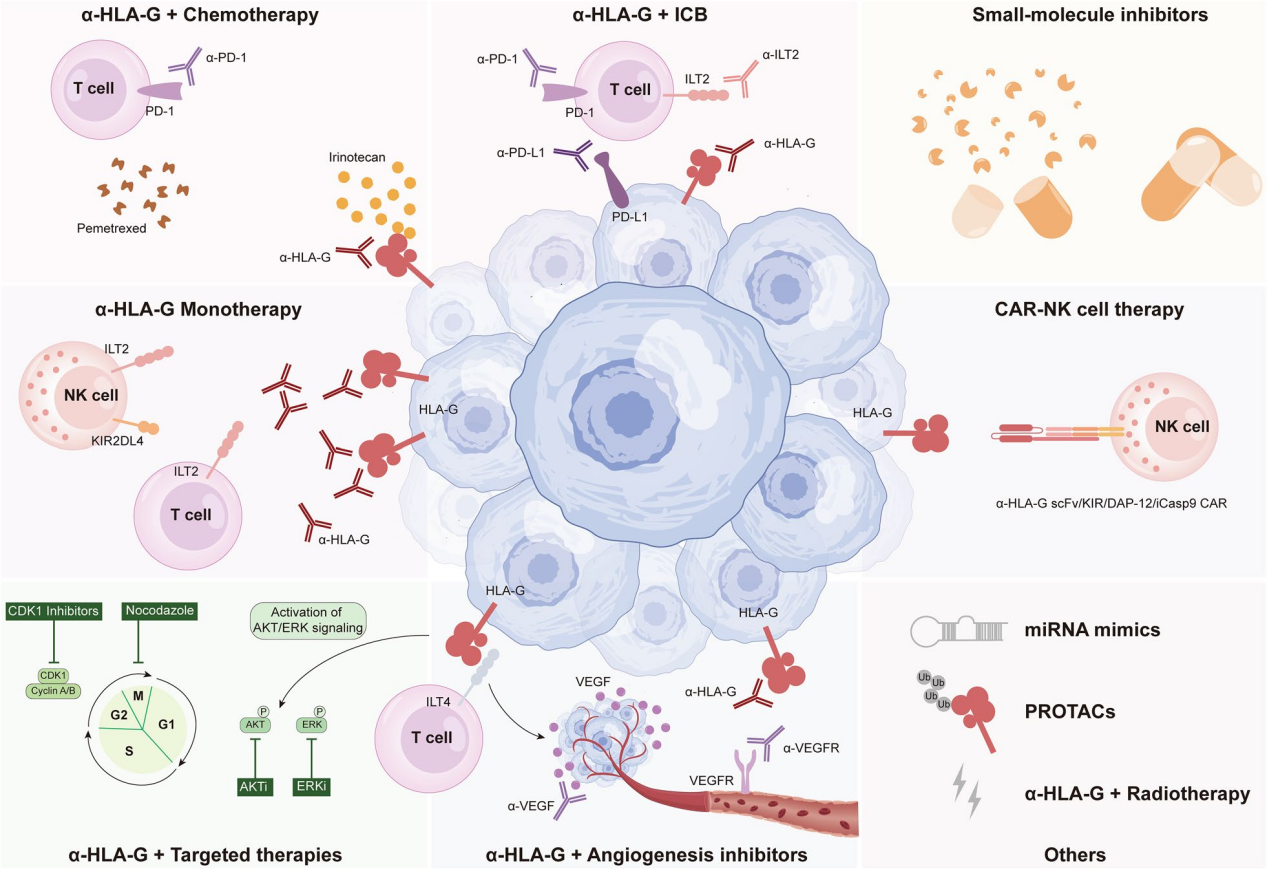
(数据来源 Wang S, et al. J Transl Med. 2024)
TTX-080是一种靶向HLAG的人源化单克隆抗体,由Tizonatx开发,TTX-080特异性地与HLA-G结合,并阻断其与ILT2和ILT4的相互作用。TTX-080正在一项随机的1b期研究中评估其与Cetuximab+FOLFIRI联合使用的情况,该研究针对的是转移性结直肠癌患者,其依据是TTX-080的单臂研究中观察到的抗肿瘤活性。


(数据来源 Tizonatx官网)
IMB-201是一种靶向HLAG的单克隆抗体,它通过阻断抑制性受体(这是肿瘤免疫逃避性的原因)的相互作用来使肿瘤微环境恢复正常,从而杀死肿瘤细胞。此外,它还被设计具有双重作用机制,通过基于HLA-G的肿瘤特异性表达(TSA)的Fc效应器功能实现额外的肿瘤杀伤效果。

利用IMB-201的优势以及针对TSA和HLA-G的靶向作用所带来的宽泛的安全性余量,imbiologics公司正试图开发一种具有增强治疗指数的全新药物,通过嫁接技术来提高IMB-201 抗体的疗效,以满足已有的免疫检查点抑制剂所无法满足的医疗需求。
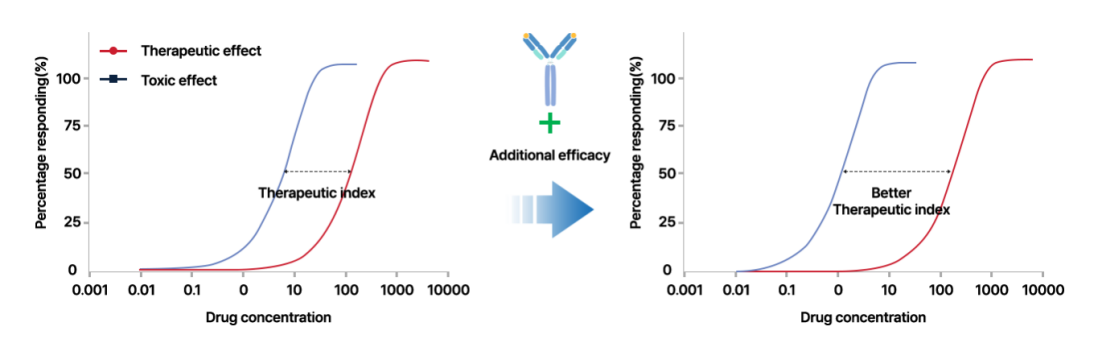
(数据来源 imbiologics官网)
我们收集整理一批HLAG相关抗体序列信息。文档可关注公众号“迈思生物”,号内回复“HLAG”下载。
