C3是补体系统的核心效应分子,通过不同的结合位点及其对应的受体介导其多种功能。补体C3是三种补体激活途径(经典途径、旁路途径和凝集素途径)的中央枢纽,C3在免疫调节,炎症调控,血管性疾病,阿尔兹海默病中发挥重要作用。

(数据来源 Batista AF, et al. Int J Mol Sci. 2024)
C3的表达分布
补体C3主要由肝脏中的肝细胞合成,并在生理状态下以无活性的前体形式分泌到血液中。C3在炎症或病理条件下也能由多种肝外组织和细胞局部产生。血管内皮细胞、屏障器官(如肠道、肺和肾脏)的上皮细胞、成纤维细胞以及包括单核细胞、巨噬细胞、树突状细胞和T淋巴细胞在内的免疫细胞,均被发现能表达C3,以响应促炎刺激如白细胞介素-1β(IL-1β)、肿瘤坏死因子-α(TNF-α)和Toll样受体配体。
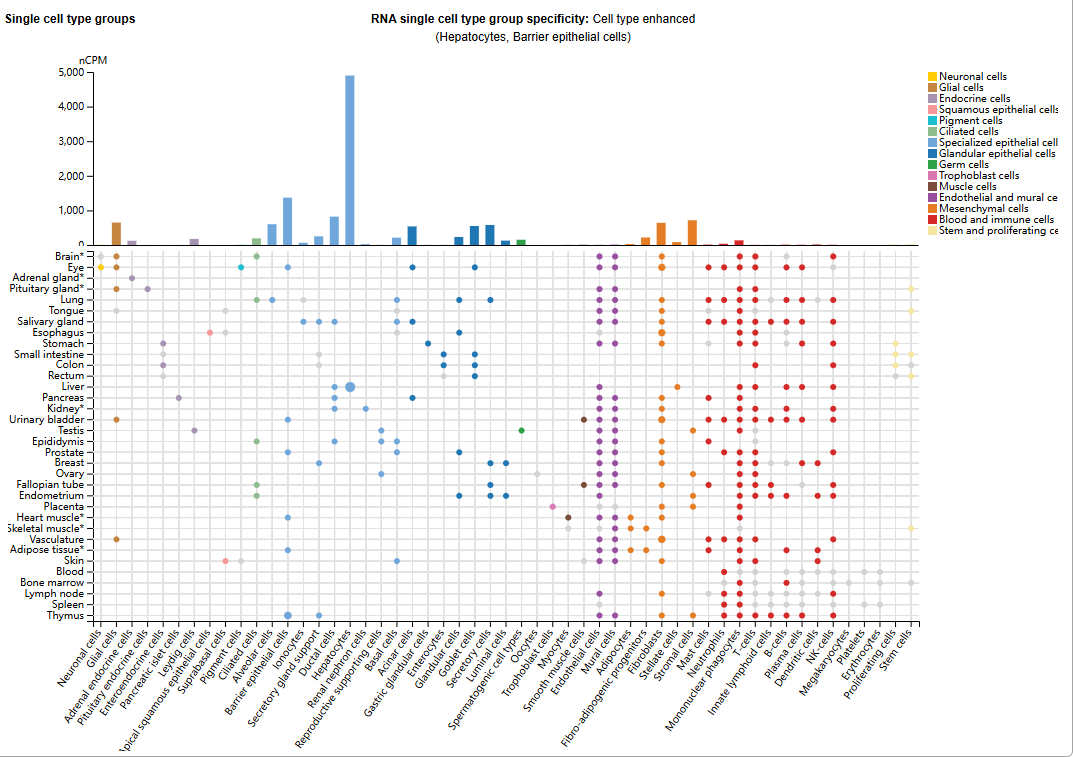
(数据来源 uniprot)
C3的结构和组成
C3是一种分泌型蛋白,主要由1663个氨基酸组成,补体C3是一种结构模块化蛋白,作为补体级联反应中的关键节点发挥作用。其结构由一条β链形成稳定的巨球蛋白(MG)核心和一条包含调节结构域的α链组成,如脱敏毒素片段、CUB结构域、含硫酯的结构域(TED)和C345c结构域。
C3前体(Pro-C3)在折叠过程中被氧化,形成13对二硫键,并在三个不同的位点(Asn-85,Asn-939,和Asn-1617)后翻译修饰为复杂的N连接糖。在从细胞中分泌出去之前,由furin蛋白酶切割pro-C3产生两个不同的多肽,通常称为β链(残基23-667;75 kDa)和α链(残基672-1663;110 kDa),它们通过分子间的二硫键在天然C3(185 kDa)中保持共价结合。尽管成熟的C3蛋白由13个不同的结构域组成,但一系列的蛋白水解反应会导致形成C3的各种片段,这些片段不仅在组成和三维结构上有所不同,而且在功能特性上也有所不同。C3可以被分解成C3a,C3b,iC3b,C3c,C3f等。
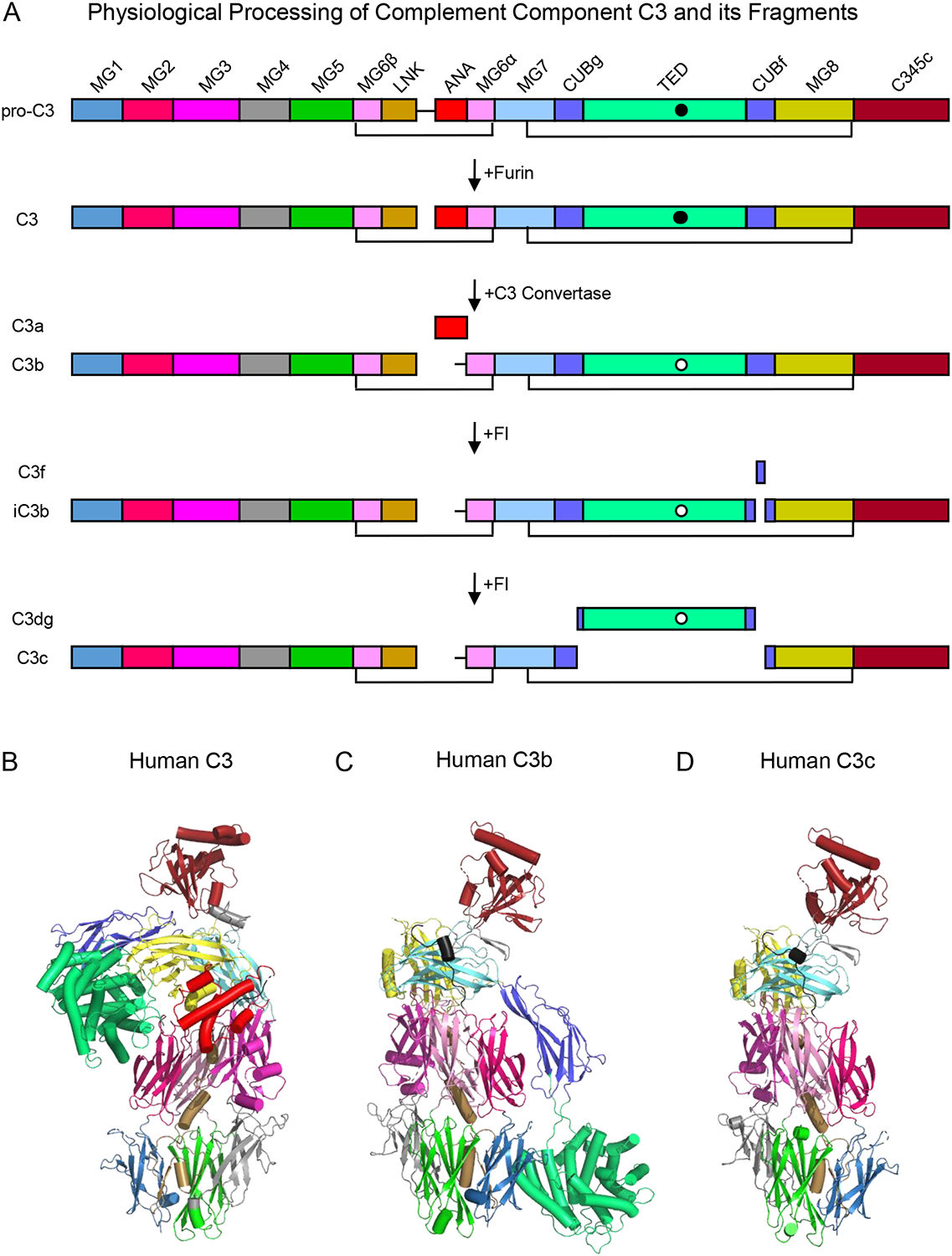
(数据来源 Geisbrecht BV, et al. Semin Immunol. 2022)
补体C3的激活
补体C3整合了三种典型途径的信号,替代途径(由病原体或改变自身触发)、凝集素途径(通过凝集素识别微生物模式)和经典途径(通过抗体-抗原免疫复合物)。补体C3由经典/凝集素途径的C3转化酶(C4b2a)或替代途径的C3转化酶(C3bBb)切割成两个主要片段,C3a和C3b。非肝细胞局部产生的C3进一步增强了补体活性。
C3a通过G蛋白偶联受体(C3aR)促进炎症,作为强效促炎介质,从而调节免疫细胞活化、趋化作用和血管通透性。
较大片段C3b经历构象重排,暴露出TED域内的反应性硫酯基团,这有助于C3b与附近的病原体表面、凋亡细胞或受损组织共价结合。表面结合的C3b在增强补体级联反应中起着关键作用,促进C5转化酶组装,并启动膜攻击复合物(MAC)的形成。C3b进一步加工成iC3b、C3dg和C3d,通过补体受体(CR1-CR4)调节免疫应答,它们在吞噬作用、免疫复合物清除、B 细胞共刺激以及通过与补体受体结合促进适应性免疫记忆中仍然保留着重要作用。


(数据来源 Li Y, et al.Clin Sci (Lond). 2025)
C3在疾病中的作用
C3在炎症和心血管疾病中的作用
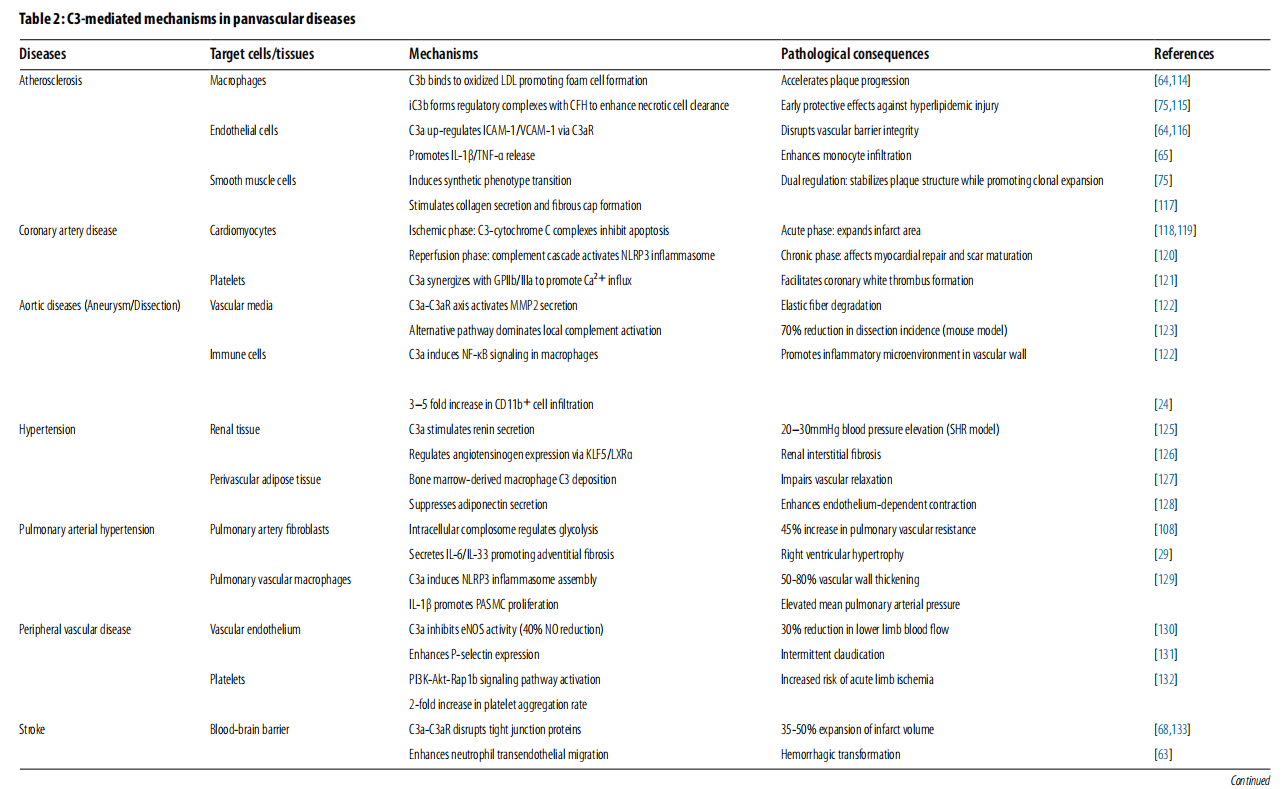
激活后,C3生成效应片段,放大炎症并启动下游级联反应,将早期免疫反应转化为结构组织损伤。除了其在免疫防御中的经典作用外,C3对涉及血管重塑的各种细胞类型具有多种影响,形成一个细胞特异性的调节网络,控制血管通透性、免疫细胞招募和组织重塑。
补体C3调节着多种细胞类型之间的免疫-血管相互作用。在内皮细胞中,C3a/C3aR信号传导会促进促炎性细胞因子的产生、白细胞黏附、细胞骨架破坏以及一氧化氮合成量的减少。在血管平滑肌细胞(VSMCs)中,C3a和iC3b会驱动表型转换、增殖和纤维帽形成,而C5a则通过基质金属蛋白酶(MMPs)诱导基质降解。在先天免疫细胞中,C3片段会增强中性粒细胞和单核细胞的募集,促进CR3介导的吞噬作用和M1型巨噬细胞的极化。在适应性免疫细胞中,细胞内的C3信号传导会调节T细胞的激活和代谢重编程,而C3d则增强B细胞的共刺激作用。与血小板结合的C3a和C5a会促进激活和血栓形成。在成纤维细胞中,C3a会诱导肌成纤维细胞转变和纤维化,而iC3b则支持树突状细胞的激活。
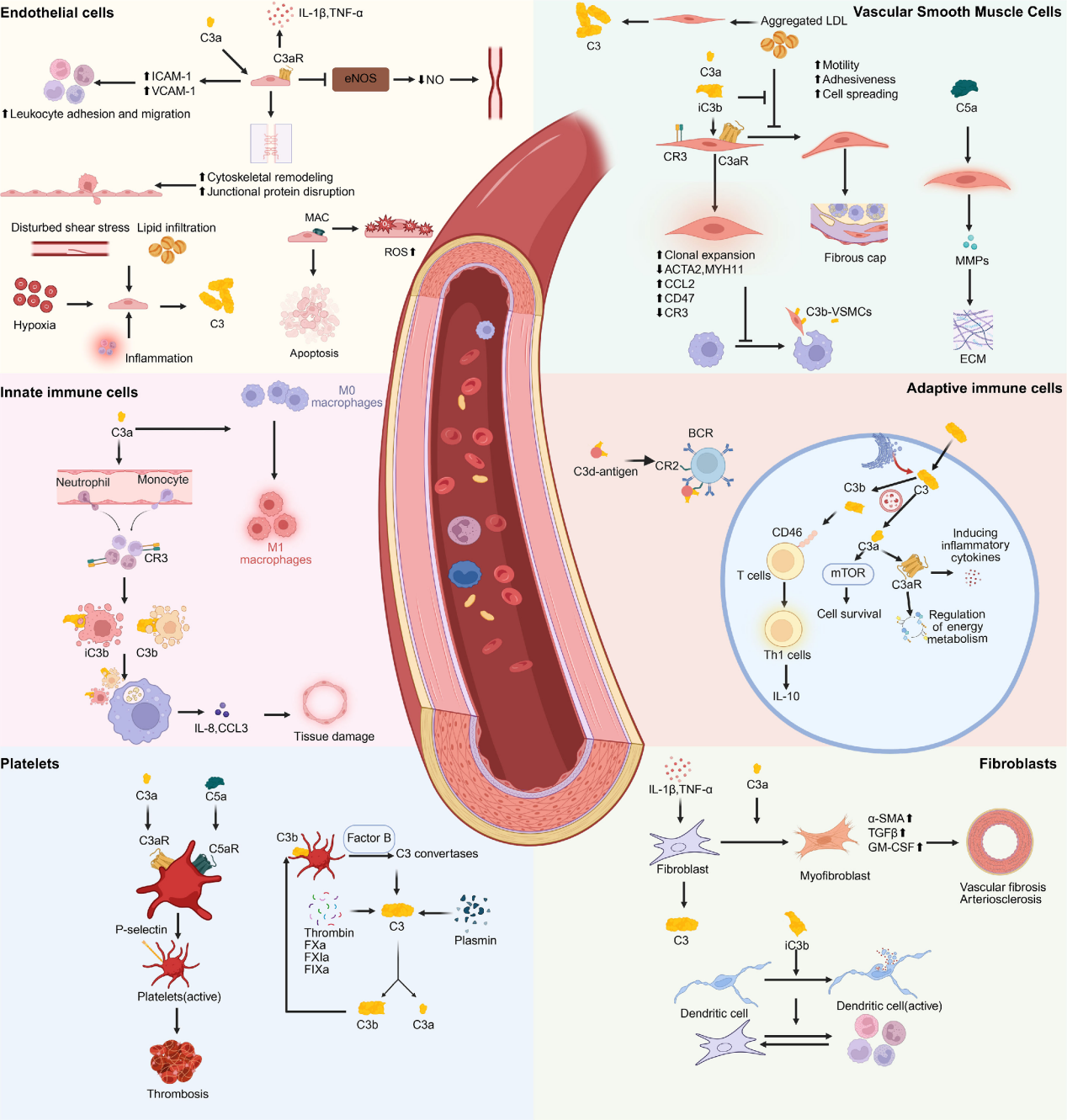
(数据来源 Li Y, et al.Clin Sci (Lond). 2025)
补体C3根据疾病阶段表现出双重效应,早期激活促进抗炎细胞因子的产生、M2巨噬细胞极化并限制下游C5激活,而在进展阶段的持续激活则驱动斑块发展、血管重塑、脂质代谢功能障碍、VSMC迁移和炎症。
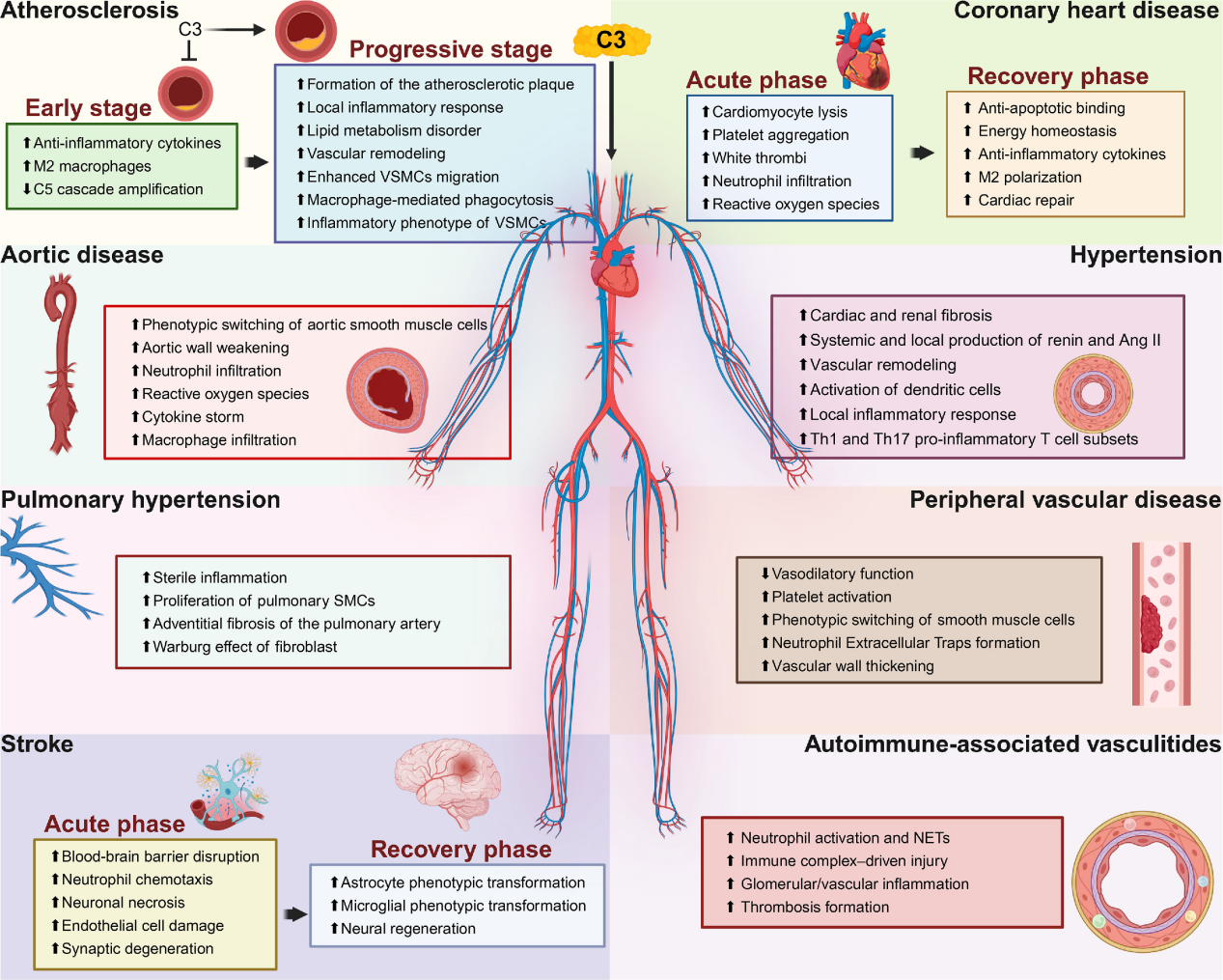
(数据来源 Li Y, et al.Clin Sci (Lond). 2025)

(数据来源 Li Y, et al.Clin Sci (Lond). 2025)
补体C3在阿尔兹海默病(AD)中的作用
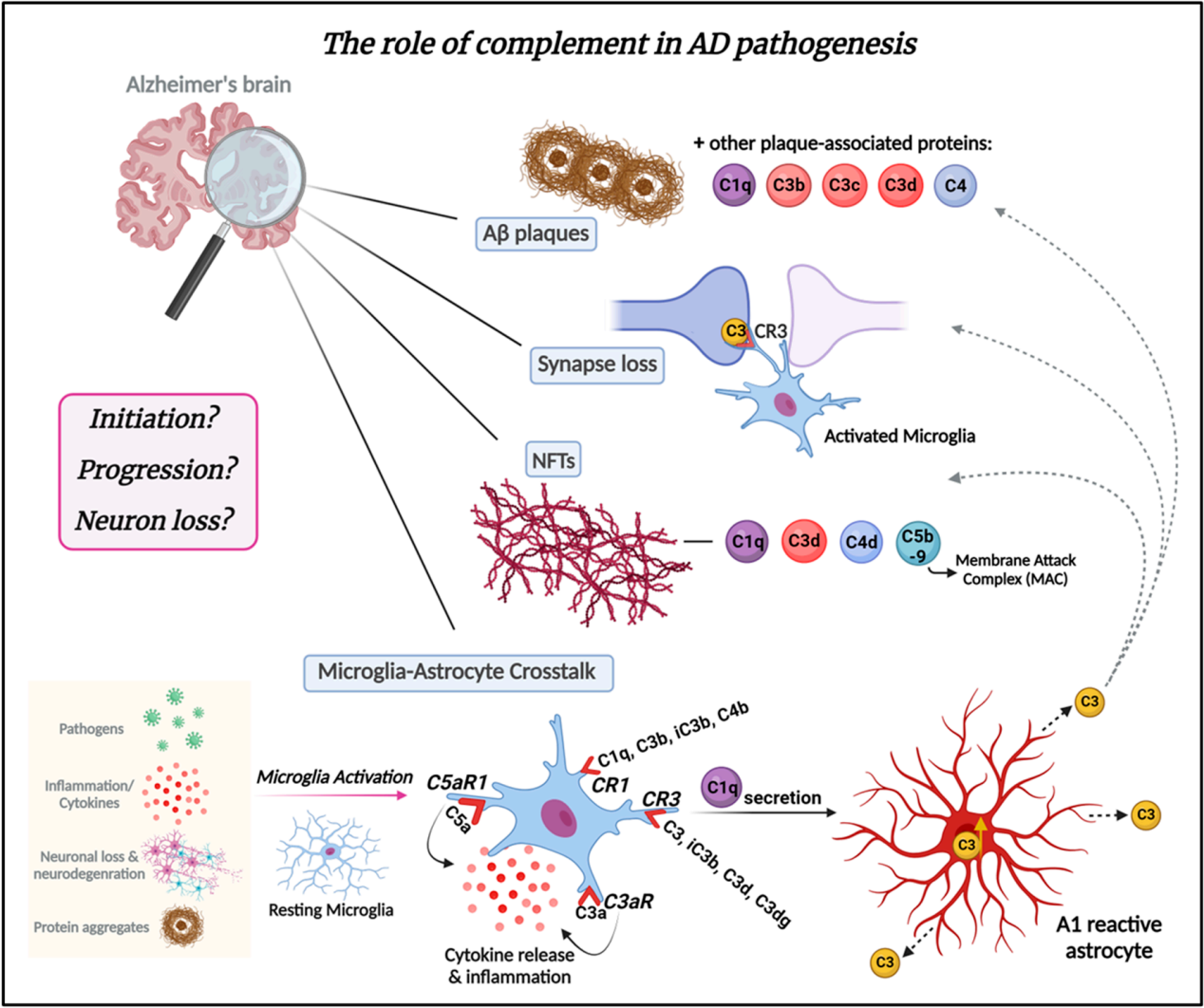
补体系统在正常大脑发育、衰老和阿尔茨海默病(AD)进展中起着至关重要的作用,通过调节突触修剪和消除以及神经元迁移。补体蛋白C1q、C3b、C3c和C3d在整个AD发病机制中与淀粉样斑块及其内的退行性神经突有关,突触丧失是AD的另一个关键特征。

补体C3/C3b在AD中通过标记弱突触并发出“吃我”信号,在突触消除中emerged为关键角色。小胶质细胞携带CR3受体,识别被标记的突触并通过吞噬作用消除它们。补体蛋白,如C1q、C3d、C4d和C5b-9,也与AD中的神经纤维缠结(NFTs)共定位。小胶质细胞和星形胶质细胞之间的串扰是AD发病机制和进展的重要组成部分,可能由补体介导。活化的微胶质细胞分泌的C1q会诱导A1反应性星形胶质细胞。A1星形胶质细胞的特点是C3表达和分泌增加。C3从A1反应性星形胶质细胞中释放出来,沉积在淀粉样斑块、弱化的突触和NFTs上。
C3在大脑发育和衰老期间也被确定为关键角色,C3水平在衰老和阿尔茨海默病(AD)患者的大脑和脑脊液(CSF)中显示出增加,并且C3的过度激活与神经损伤有关。在神经炎症期间,C3可能在促进突触损伤方面发挥关键作用。在C1q引发经典补体级联反应之后,C3被激活,从而清除病原体。因此,敲除或抑制C3(这将抑制补体激活的所有下游成分)可能成为多种疾病(包括阿尔茨海默病)的有前景的治疗靶点。
(数据来源 Batista AF, et al. Int J Mol Sci. 2024)
C3的靶向治疗
LP-005是longbio开发一种靶向C3b和C5的双功能抗体融合蛋白,在补体抑制(CP)、抗原抑制(AP)和补体抑制(LP)和C3b沉积检测中具有更好的生物活性。同时,LP-005被设计用于优化表面电荷(PI)和FcRn结合,使其成为全球首个Q4W双功能补体抑制剂。LP-005主要用于治疗阵发性夜间血红蛋白尿(PNH),补体介导的肾脏疾病和其他补体相关疾病。

(数据来源 longbio官网)
CG001是由上海康景生物医药科技有限公司研发的靶向C3的抗体融合蛋白,它在补体激活的核心C3水平发挥细胞靶向性补体抑制作用,不但可高效抑制补体经典和凝集素途径的激活,且可更高效抑制补体旁路途径的激活,从而有效阻止所有补体活性产物包括C3a/C5a、C3b/iC3b和C5b-9n(MAC)的产生或功能,在包括重症肌无力在内的多种疾病模型中对补体过度激活性疾病显示出异常优异的疗效。CG001已获得中国NMPA和美国FDA临床批件开展临床研究。
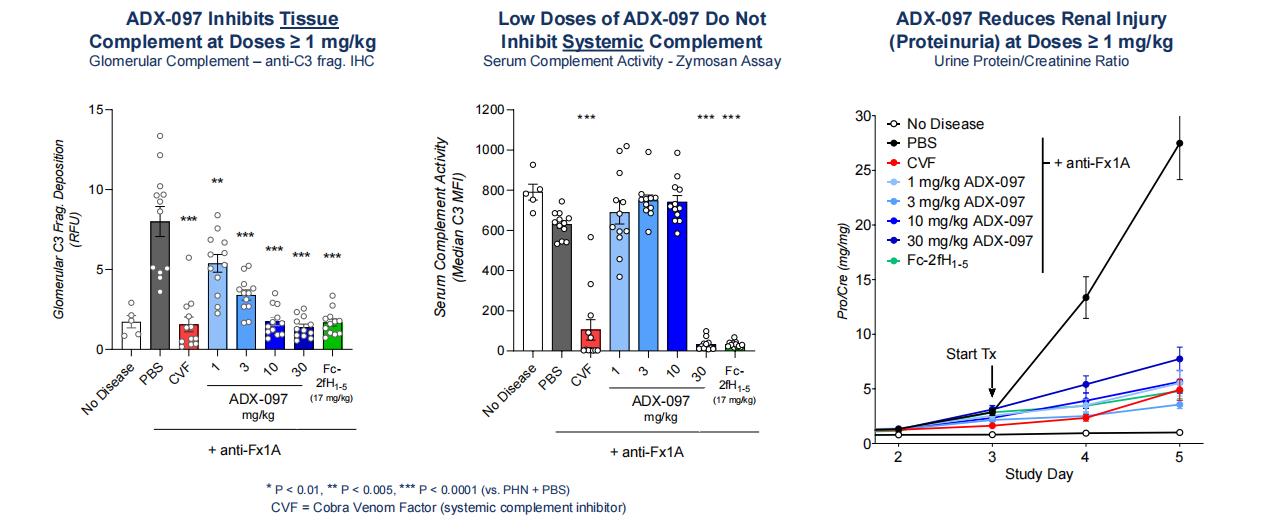
ADX 097是Q32 Bio开发的一款靶向C3d的融合蛋白,处于临床1期研究阶段,用于治疗自身免疫性疾病,抗中性粒细胞胞质抗体相关性疾病。ADX-097提供了一种独特的靶向治疗方法,能够在病变组织中抑制替代途径(AP)的激活,同时最大限度地减少全身补体阻断。ADX-097是一种双功能融合蛋白,包含人类因子H的前五个共有序列(fH1-5)的两个部分与一种人源化抗C3d抗体连接在一起。ADX-097旨在通过与补体激活部位沉积的C3d 结合来靶向病变组织,并提供局部阻断作用。ADX-097能降低蛋白尿,并抑制肾小球中的补体活性,其用药剂量不会影响全身的补体活性。

(数据来源Q32 Bio官网)
我们收集整理一批C3相关抗体序列信息。文档可关注公众号“迈思生物”,号内回复“C3”下载。
