粘蛋白按结构分为四类,包含串联重复序列(TR)的膜限制性粘蛋白,富含半胱氨酸的分泌型粘蛋白(包含TR序列),半胱氨酸缺乏的分泌型粘蛋白(含TR序列),无TR序列的粘蛋白。MUC5A是一种富含半胱氨酸的分泌型粘蛋白,是一种胃和呼吸道上皮的凝胶状糖蛋白,这种粘蛋白赋予黏液其特有的粘弹性,这一特性对于纤毛细胞清除外源性物质至关重要。MUC5A的信号转导受炎症因子与生长因子等上游因子调控,影响细胞增殖、凋亡、迁移与侵袭等下游效应分子。在疾病方面,与哮喘、慢性阻塞性肺疾病、胃癌、肠炎等多种疾病密切相关。针对MUC5A的靶向治疗,包括小分子抑制剂及基因治疗策略,展现出潜在应用前景。

(数据来源 Li J, et al. Molecules. 2020)
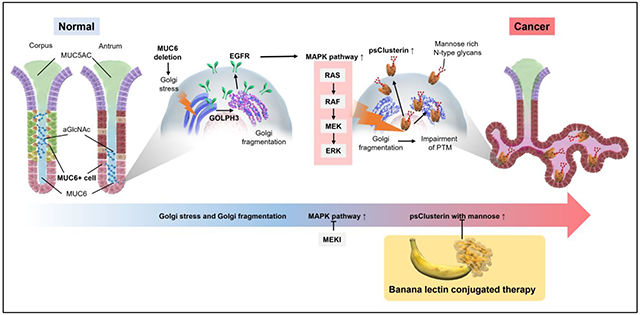
(数据来源 Arai J, et al.Gastroenterology. 2024)
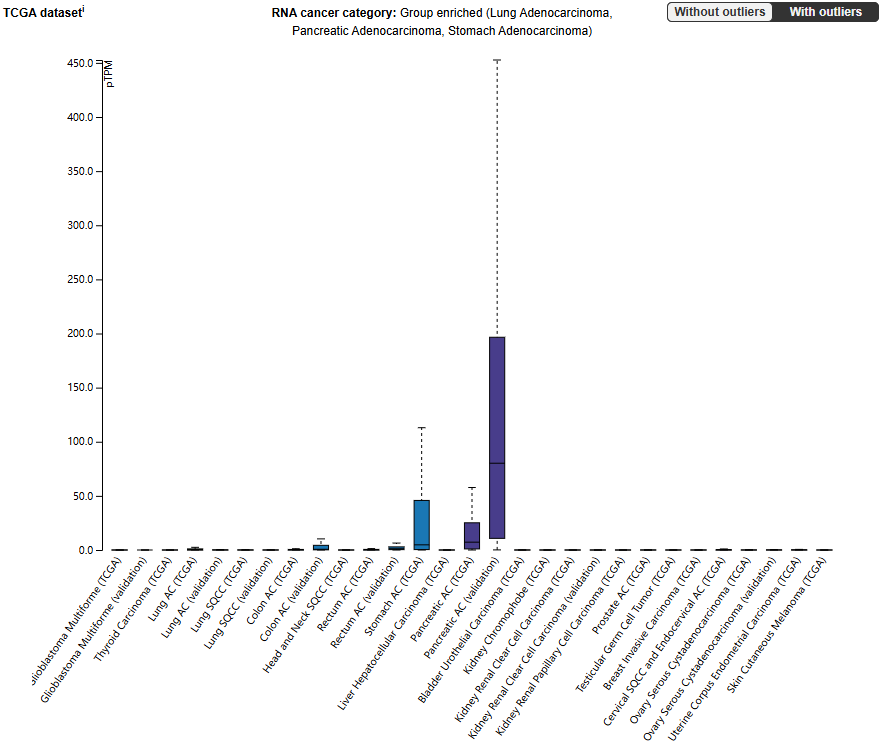
MUC5A的表达分布
MUC5A表达具有组织特异性,在呼吸道表面粘膜细胞和胃上皮细胞中高表达。在许多癌变中过表达,例如肺腺癌、胰腺腺癌、胃腺癌。在气道上皮细胞中,细胞分化过程中(在蛋白质水平上)表达显著增加。
MUC5AC可能是一个重要的生物标志物,因为这种蛋白质在胎儿和癌前结肠粘膜中表达,但在正常结肠中的表达程度较低。MUC5AC抗原的过度表达与胰腺癌和结直肠癌有关。MUC5AC在结肠癌中以异常糖基化的形式表达。

(数据来源 uniprot)
MUC5A的结构
MUC5A由5654个氨基酸组成,属于分泌型黏蛋白中的成胶型黏蛋白。MUC5A的N端VWD1和VWD2等结构域通过与相邻分子的C8结构域相互作用,组装成“珠状”单元,进而形成线性纤维,这是构成粘液凝胶网络的基础。其中,VWD3结构域可通过形成共价二聚体并进一步组装为四聚体,驱动形成网状聚合物。
中央区域是富含脯氨酸、苏氨酸和丝氨酸的PTS结构域,该区域被高度O-糖基化,形成刚性的“棒状”结构。MUC5A的PTS区域被多个富含半胱氨酸的CysD结构域(共9个,即CysD1至CysD9)分隔。这些结构域参与同型相互作用,对粘液结构进行精细调节。
MUC5AC基因的高度多态性导致了其结构域的拷贝数存在个体差异,影响蛋白长度,这可能导致个体间粘液屏障特性的差异。

(数据来源 Haberman M, et al. Proc Natl Acad Sci U S A. 2025)
MUC5A疾病中的作用
MUC5A在慢性阻塞性沛病中的作用
慢性阻塞性肺疾病(COPD)在全球范围内具有较高的发病率和死亡率。慢阻肺也被认为是一种粘液阻塞性疾病,伴随着粘蛋白含量增加,特别是MUC5AC它可能独特地改变粘液的特性。MUC5AC可导致严重的黏液阻塞性肺疾病,加重COPD的发病机制。MUC5AC的异常产生和分泌涉及多种途径。
在慢性阻塞性肺疾病(COPD)中,细胞外的信号因子,如肿瘤坏死因子-α(TNF-α),会与细胞表面受体结合,从而引发一系列下游反应。受体刺激会触发IκB激酶(IKK)的激活。IKK会磷酸化细胞内NF-κB的IκB亚基的调节位点的丝氨酸,使IκB亚基发生泛素化并被降解。这进而释放出NF-κB复合物,随后游离的NF-κB移至细胞核内,在那里它驱动靶基因的表达,包括 MUC5AC。
IL-13-STAT6-SPDEF-MUC5AC信号通路是驱动上皮细胞分化为杯状细胞的主要信号通路。的一项研究发现,敲低SPDEF可减少IL-13诱导的人气道上皮细胞中MUC5AC的表达。

(数据来源 Li J, et al. Molecules. 2020)
MUC5A在癌症中的作用
MUC5A在胰腺导管腺癌(PDAC)的癌变和药物敏感性中起着至关重要的作用,在正常的胰腺细胞中,MUC5AC的生成会被抑制,并在受到适当刺激后重新启动。根据刺激的性质不同MUC5AC的组成以及由此导致的分布位置和产生水平可能会有所差异。如果刺激具有潜在的恶性特征则会产生更高水平的成熟MUC5AC,并伴随有异常的排列现象。具有较差治疗应答能力和更糟糕预后效果的侵袭性肿瘤,往往相较于良性肿瘤而言,其顶端和细胞间区域较少出现成熟的MUC5AC。如果刺激导致出现癌前或良性状态,则会产生更多处于未成熟状态的MUC5AC,且其排列过程受到控制。在发生恶性转化过程中,MUC5AC的组成和分布位置会发生变化。

(数据来源 Manne A, et al.Int J Mol Sci. 2023)
胃癌(GC)是全球癌症相关死亡的主要原因之一,存在多种表型变异,可根据黏蛋白的表达将其分为胃型和肠型。免疫组化标志物如MUC5AC和MUC6(表示胃型)、MUC2和CD10(表示肠型)有助于将胃癌病例分为四种亚型,胃型、肠型、胃肠混合型以及既不符合胃型也不符合肠型特征的类型。早期胃癌通常表现为胃黏蛋白表型。随着肿瘤的进展,从胃黏蛋白表型到肠黏蛋白表型的明确转变变得更加明显。粘蛋白和粘蛋白相关糖的改变有可能影响GC以外各种癌症类型的癌变。MUC6的缺失会引发高尔基体应激反应,并上调GOLPH3的表达,从而导致EGFP/MAPK的激活。αGlcNAc的缺失会导致MUC1C末端的磷酸化,从而促进Src和β-连环蛋白与由半乳糖凝集素-3引起的该C末端的结合。胃上皮O糖基的缺乏会导致caspases 1和11依赖性炎症小体的激活,从而导致胃炎和胃癌的进展。这还会通过RON通路激活或Wnt通路增强CD44与癌症相关的功能,同时激活EGFR、ErbB2、SRPX2和RUNX1。MUC5AC的缺失会导致Tff1、Tff2和Muc1的表达增加,而Tnf和Il17a的表达减少。MUC2的缺失会导致细胞间连接缺陷、线粒体损伤以及肠上皮内的ATP耗竭。

(数据来源 Arai J, et al. Cancer Sci. 2024)
MUC5A的靶向治疗
Ensituximab(NEO-101)是一种靶向MUC5A的新型嵌合抗体,治疗结肠癌。Ensituximab能够区分异常糖基化的形式与天然的MUC5AC。临床前数据表明,Ensituximab仅靶向MUC5AC阳性肿瘤,并且不损伤非恶性组织中的MUC5AC抗原。单臂、II期试验评估了Ensituximab在表达MUC5AC抗原的晚期、难治性癌症患者中的疗效和安全性。Ensituximab以每2周3 mg/kg的推荐II期剂量(RP2D)静脉给药。Ensituximab在结直肠癌患者中耐受性良好,并显示出一定的抗肿瘤活性。
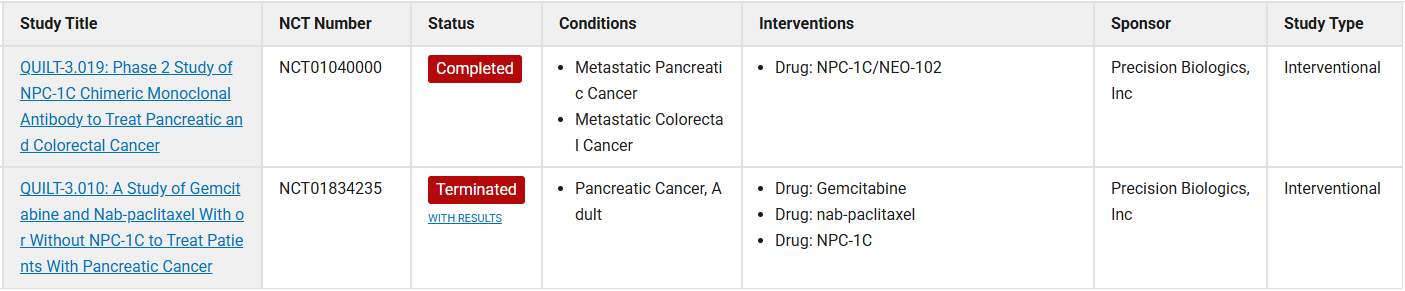
(数据来源 clinicaltrials)

(数据来源 Kim RD, et al. Clin Cancer Res. 2020)
我们收集整理一批MUC5A相关抗体序列信息。文档可关注公众号“迈思生物”,号内回复“MUC5A”下载。
