GDNF家族有四个成员,分别是GFRα1、GFRα2、GFRα3和GFRα4,它们通过含有细胞外囊泡结合域(CRD)的细胞外囊泡锚定结构连接到细胞膜上。GDNF家族配体(GFLs)具有四种特征性配体,即GDNF、NRTN、ARTN和PSPN。两个GFL单体形成相互缠绕的同源二聚体,与相应的GFRα受体结合体相结合。GFRA3是GDNF家族受体α-3,它主要与视网膜母细胞瘤蛋白受体(ARTN)结合,ARTN一种支持感觉和交感周围神经元存活的生长因子。ARTN结合导致RET受体的自磷酸化和激活。GFRA3因其介导神经病理性疼痛和在肿瘤进展中的潜在作用,已成为一个极具潜力的治疗靶点。目前,针对该靶点的研究主要集中在开发抗体药物以阻断疼痛信号,或探索其在肿瘤靶向治疗中的应用。
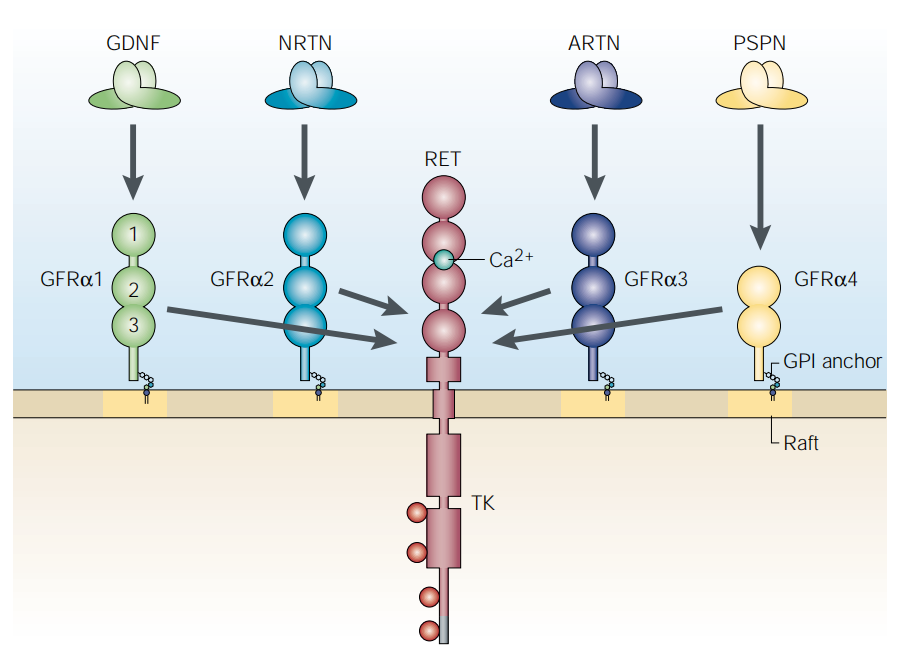
(数据来源 Airaksinen MS, et al. Nat Rev Neurosci. 2002)
GFRA3的表达分布
GFRA3主要表达在神经胶质细胞、肠内分泌细胞、卵母细胞、生精细胞类型。在成人和胎儿中广泛表达,表现出相似的模式。在中枢神经系统中基本不表达,但在外周神经系统的几个感觉和交感神经节中高度表达。在许多非神经组织中有中等表达,特别是消化系统和泌尿生殖系统,但在胃和阑尾中有高表达。几种类型的腺组织表现低表达。在造血系统中检测到极低或无表达。
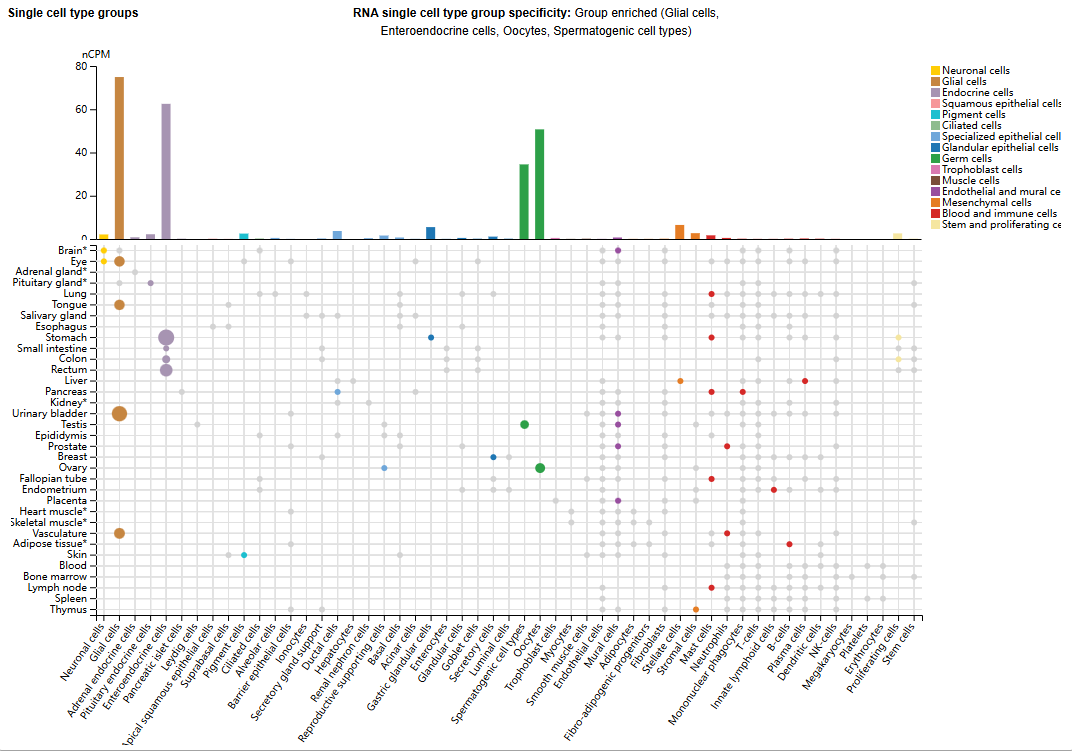
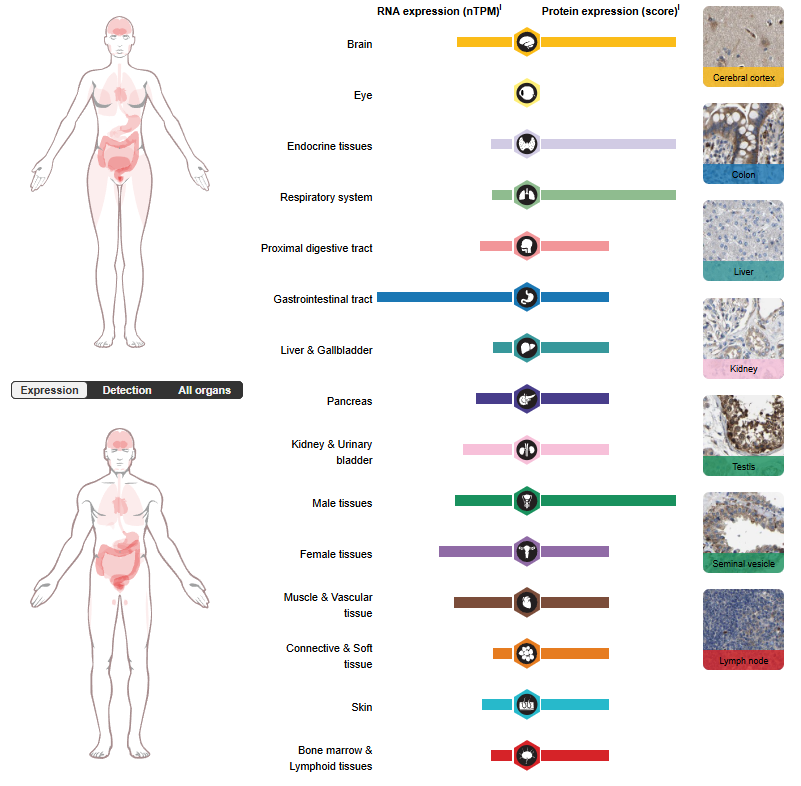
(数据来源 uniprot)
GFRA3的结构和信号转导调控
GFRA3属于糖基磷脂酰肌醇(GPI)锚定的细胞表面蛋白,由400个氨基酸组成。它主要由信号肽,胞外结构域和GPI锚定结构构成。胞外结构域包含两个CUB结构域和一个GFRα特有结构域,负责配体识别。GPI锚定结构是无跨膜结构域,通过GPI锚定在细胞膜外侧,限制其在膜上的流动性。
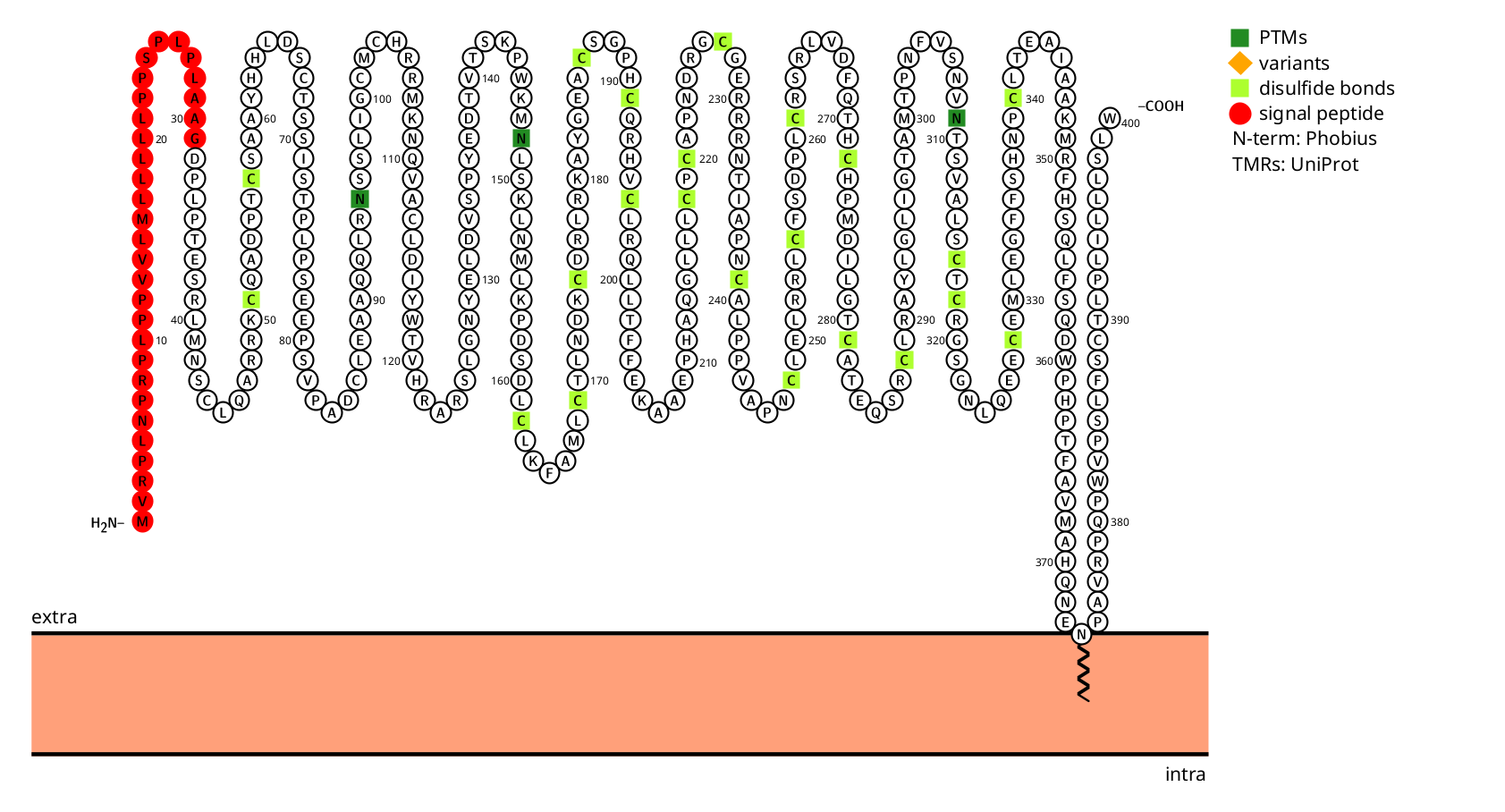
(数据来源 protter)
在GFL和GFRα结合后,复合物与RET(一种跨膜酪氨酸激酶受体)结合,形成GFL-GFRα-RET三元复合物。GFRA3其信号传导依赖于“配体-受体-共受体”的三元复合物模式。依赖于RET的GFRα信号传导是通过GFRα在多个细胞内酪氨酸上的磷酸化而激活的。Ras/MAPK和PI3K/Akt信号通路两种信号转导途径有助于GFL诱导的RET激活:通过膜结合的GFRα(顺式信号传导)和从附近细胞释放的可溶性GFRα(反式信号传导)分子。GDNF的存在促进了CFRα与NCAM的结合,从而激活了由NCAM介导的Fyn-FAK-MAPK信号通路。
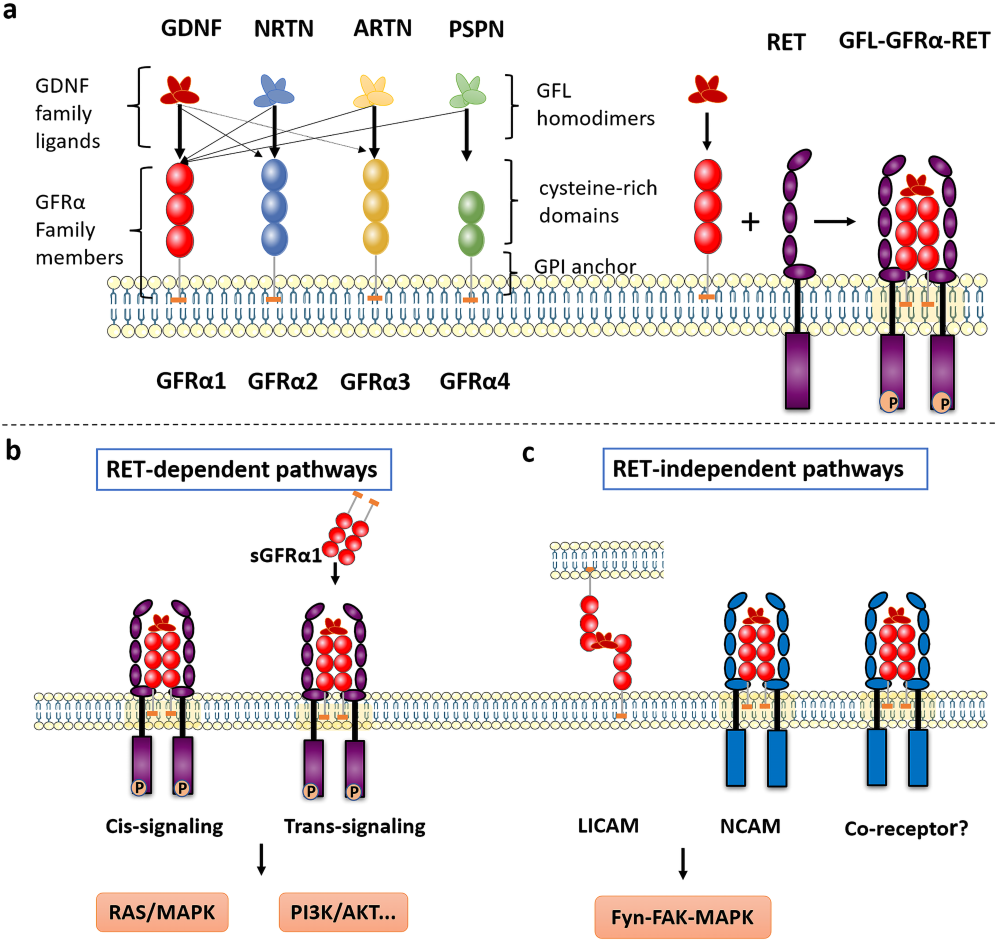
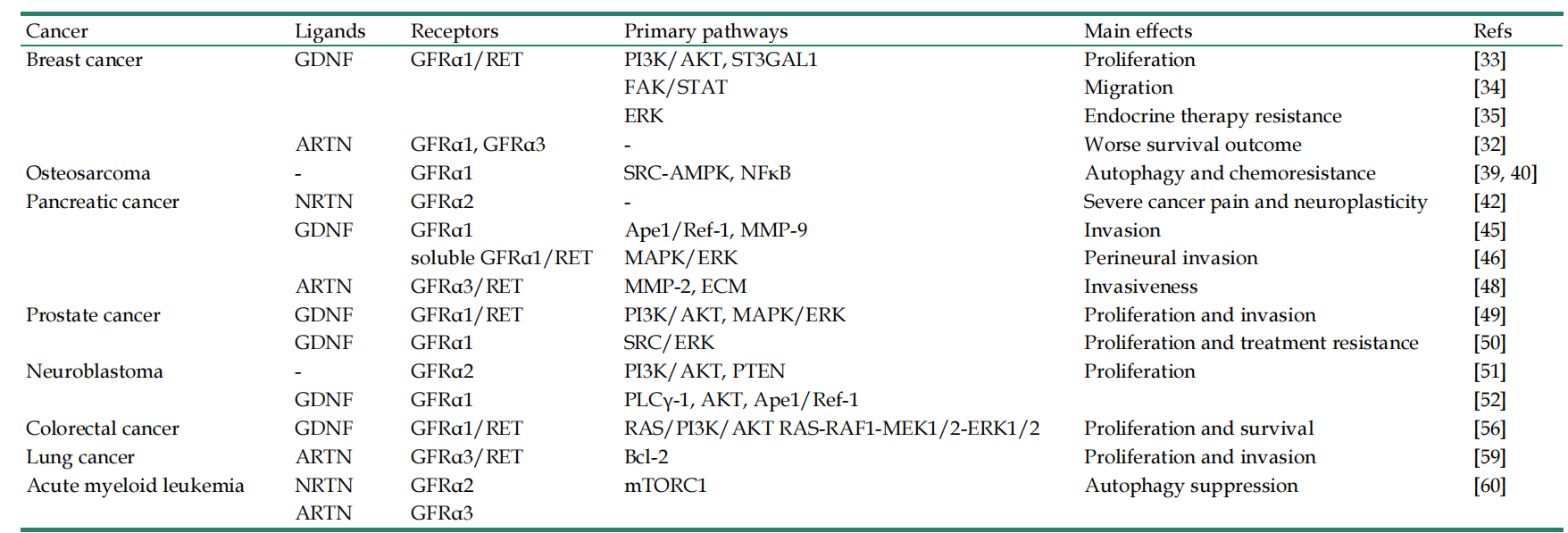
(数据来源Li Q, et al. Int J Med Sci. 2022)
GFRA3在疼痛中的作用
GFRα3在持续性疼痛(包括肌肉骨骼疼痛)中发挥重要作用,因此是开发新型临床有效的肌肉骨骼疼痛镇痛药的潜在治疗靶点。GFRα3是Artemin(ARTN)介导的慢性肌肉骨骼疼痛(尤其是OA疼痛和炎性骨痛)的关键受体。Artemin/GFRα3信号通过激活RET受体及下游MAPK、PI3K/AKT等通路,增强TRPV1/TRPA1等离子通道的表达与活性,介导热痛觉过敏、冷异常性疼痛及机械超敏反应。在骨关节炎和炎性骨痛动物模型中,阻断Artemin或GFRα3可减轻Aδ和C纤维对机械压力的敏感性,逆转负重行为异常及热/冷痛觉过敏,提示该信号轴在慢性肌肉骨骼疼痛中起关键驱动作用。Artemin可通过上调TRP通道(如TRPV1、TRPA1)表达,增强神经元的兴奋性,促进疼痛持续。GFRα3介导的信号在神经病理性疼痛中呈现双向效应,一方面促进神经再生与修复(如neublastin临床研究),另一方面参与冷异常性疼痛的维持(如奥沙利铂诱导的神经病变),靶向该受体需平衡镇痛与神经保护功能。
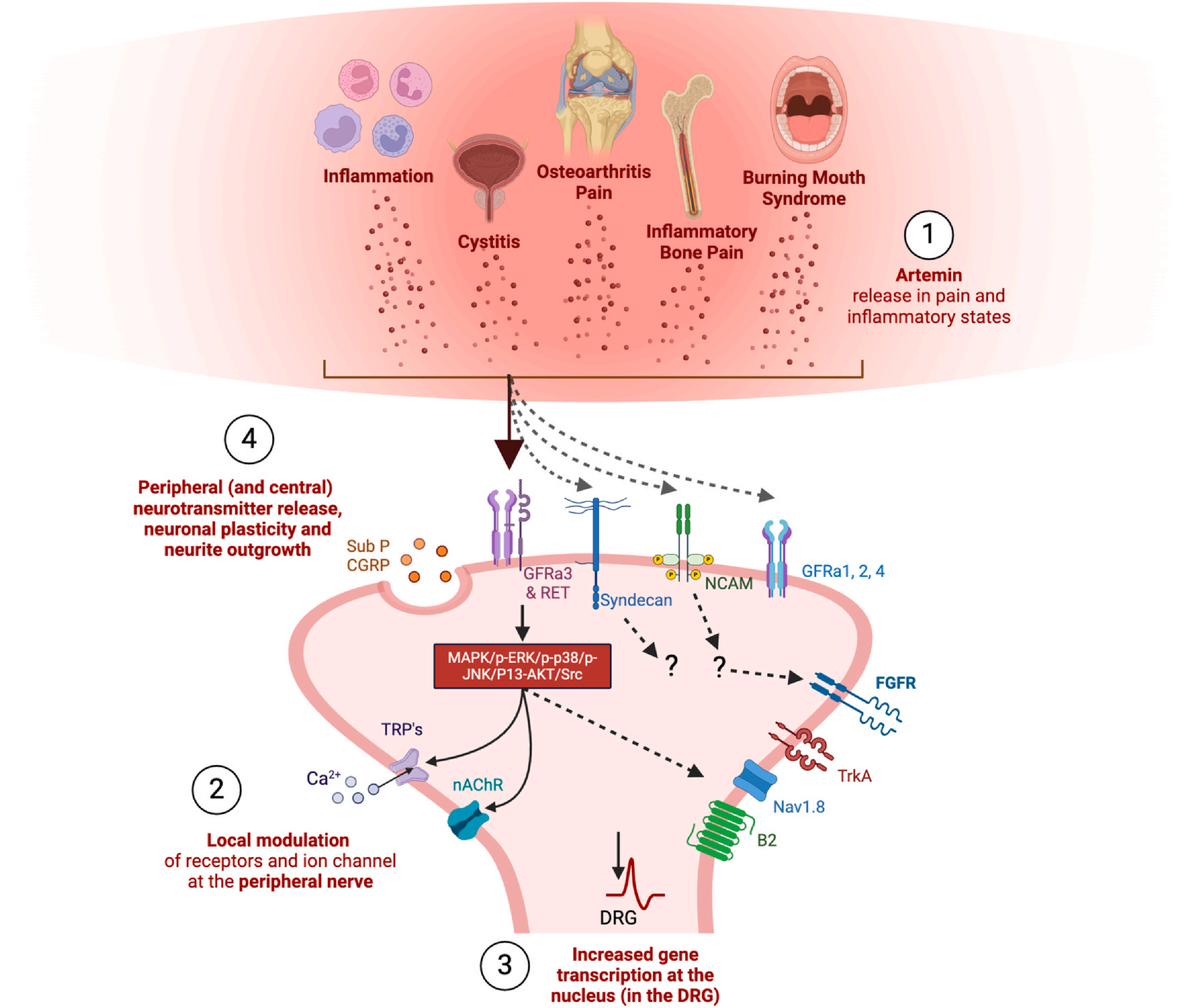
(数据来源Gupta A, et al.Osteoarthritis Cartilage. 2025)
GFRA3的靶向治疗
Nadecnemab(REGN5069)是一种靶向GFRA3的单克隆抗体,由再生元开发,用于治疗疼痛,最高研发阶段是临床2期,但是目前已经终止。
我们收集整理一批GFRA3相关抗体序列信息。文档可关注公众号“迈思生物”,号内回复“ GFRA3”下载。
