服务支持
迈思生物承担了STIM1和TFR1的蛋白表达服务。

背景
脑出血(ICH)占全球所有卒中病例的10%-15%,是疾病负担最大的卒中亚型,死亡率和致残率高达30%-80%。ICH的治疗效果并不令人满意。即使早期微创清除原发性血肿,超过50%的幸存者仍然患有中度至重度神经功能障碍,这主要是由于血肿及其代谢物引起持续性继发性脑损伤(SBI),导致不可逆的神经元损伤。血肿代谢物诱导的铁死亡是ICH后神经元死亡的主要形式,并且在SBI的进展中起着关键作用。由于脑出血(ICH)往往预后不良,需要探索有效的治疗靶点。基质相互作用分子1(STIM1)是细胞钙稳态的重要调节因子,但其在ICH中的具体作用仍不清楚。

2026年2月17日西京医院-张洪晨团队在Cell Rep Med上发表了一篇名为“The Ca2+ sensor STIM1 promotes neuronal ferroptosis by regulating iron homeostasis to exacerbate brain injury after intracerebral hemorrhage”的研究,这项研究发现ICH后神经元中STIM1持续升高,患者血浆水平升高与预后不良相关。敲除小鼠STIM1的神经元可改善脑组织损伤和神经损伤。从机制上讲,STIM1主要通过促进铁死亡来加剧神经元损伤。重要的是,除了调节钙信号通路外,STIM1还通过与转铁蛋白受体1(TFR1)的相互作用直接调节铁稳态,促进铁死亡。最后,通过虚拟筛选,S-IN-1被确定为一种针对STIM1-TFR1相互作用的抑制剂,可预防神经元铁死亡和脑损伤。这些发现证实了STIM1在调节铁稳态方面的分子功能,为ICH治疗提供了宝贵的见解和有希望的靶点。
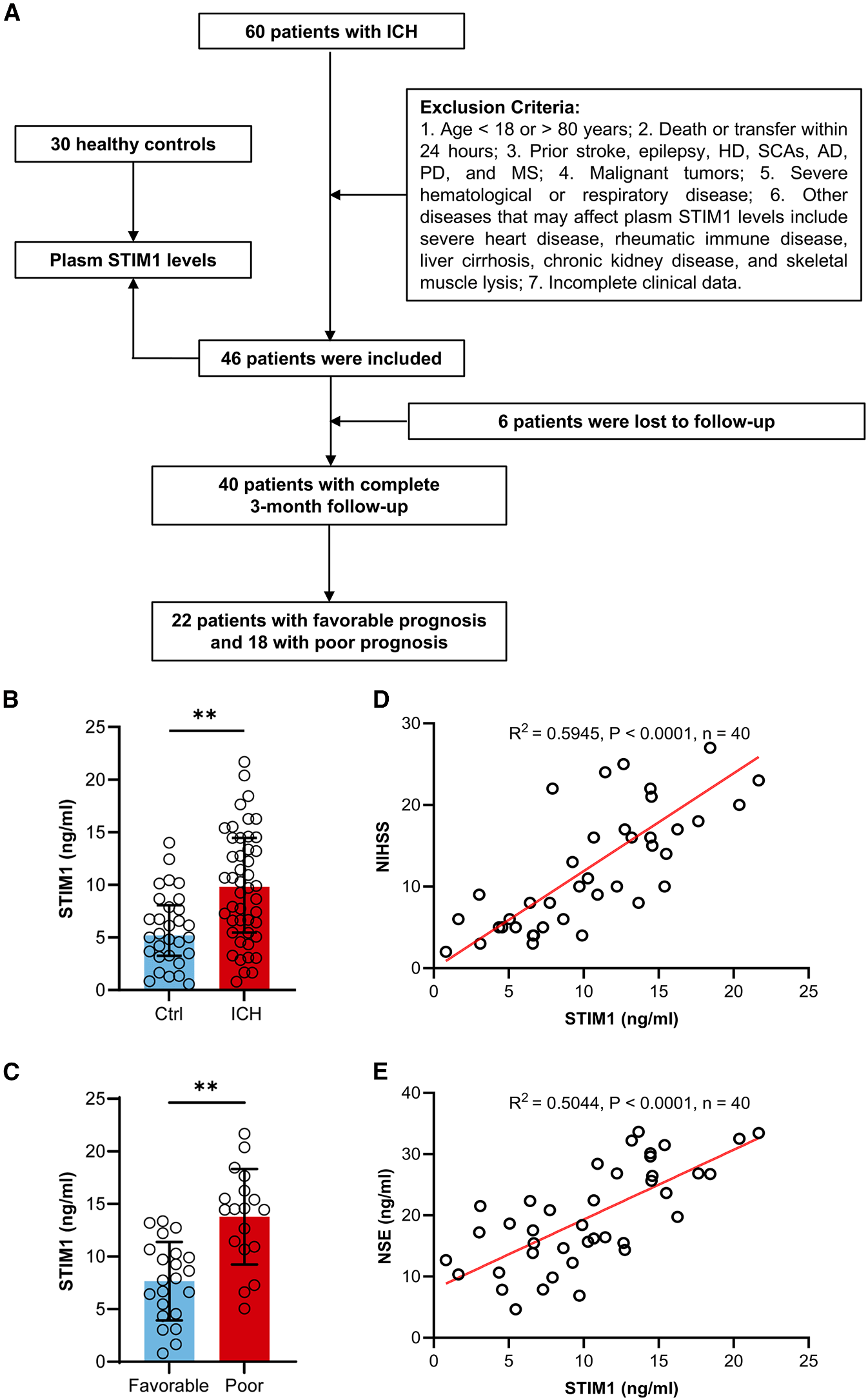
STIM1表达在ICH后上调与预后不良有关
脑出血(ICH)会诱导神经元STIM1表达增加,且预后不良的ICH患者的血浆STIM1水平高于预后良好者,血浆STIM1水平与神经元特异性烯醇酶(NSE)水平呈正相关,表明STIM1参与ICH后神经元损伤过程。这些结果表明,ICH患者的血浆STIM1水平显著升高,且出院后预后较差。

神经元STIM1基因敲除改善ICH后的脑损伤
通过Cre-LoxP重组方法生成的神经元STIM1敲除小鼠,STIM1cko小鼠表现出较轻的脑水肿,更多的存活神经元和较低的血浆NSE水平。行为实验表明,STIM1cko持续改善了修改后的神经严重程度评分(mNSS)和感觉、运动和认知神经缺陷。神经元STIM1缺失在ICH后减轻了脑组织损伤和神经损伤。

STIM1基因敲低抑制了ICH后的神经元铁死亡
STIM1敲低显著减轻了脂质过氧化的程度。STIM1敲低还显著降低了丙二醛(MDA)、4-羟基bada(4-HNE)和活性氧(ROS)的水平。此外,STIM1沉默增加了关键的铁死亡抗性因子GPX4的表达和活性,并降低了还原型谷胱甘肽/氧化型谷胱甘肽(GSH/GSSG)的比率。体外和体内实验结果,STIM1沉默有效减少了铁积累STIM1敲低在ICH后有效抑制神经元铁死亡。

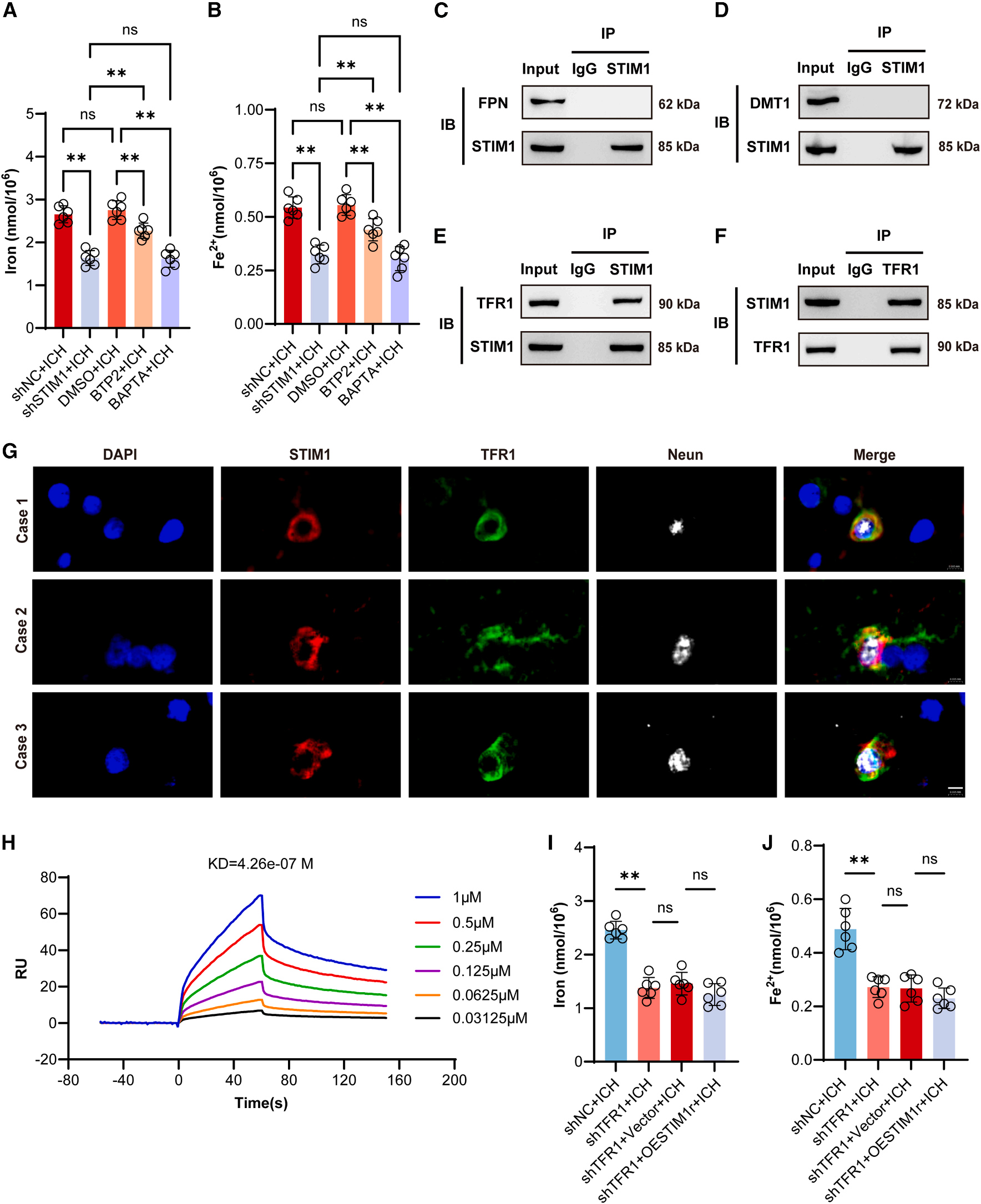
STIM1通过与TFR1相互作用调节ICH后的神经元铁稳态
通过真核表达系统构建了纯化的STIM1-CD和TFR1-CD蛋白,并通过coIP,免疫荧光共定位,表面等离子体共振(SPR)等实验验证了它们的直接相互作用。STIM1过表达在ICH后并不影响TFR1敲低的HT22细胞中的铁积累,这些结果表明,STIM1在ICH后与下游靶标TFR1相互作用,以调节神经元的铁稳态。
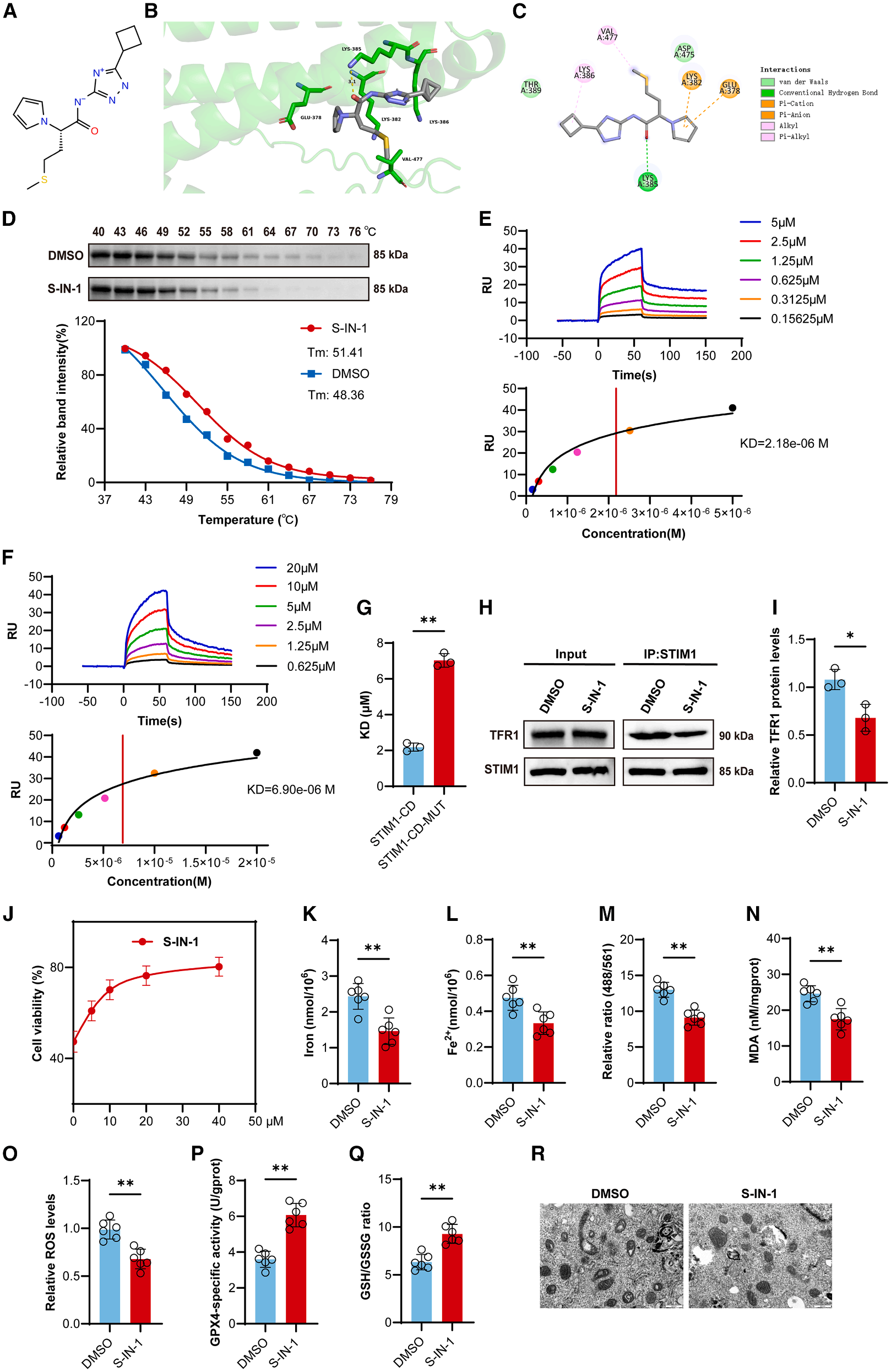
STIM1通过增强TFR1活性促进铁内流
通过分子对接和动力学模拟发现STIM1链A的Lys385位点贡献了最高的ΔG结合,并且仍保持与TFR1、Glu44和Glu45的氢键相互作用。通过对STIM1 Lys385突变,STIM1 MUT与TFR1在STIM1敲低细胞中的相互作用显著减少。STIM1 MUT降低了FL-TF的摄取,STIM1 Lys385突变还削弱了STIM1-ORAI1的相互作用以及SOCE。但SOCE抑制不会影响STIM1-TFR1结合、TFR1表达或TFR1活性,表明STIM1-TFR1相互作用介导的铁摄取是独立于STIM1/ORAI1介导SOCE的生物学过程。这些结果说明STIM1可以通过SOCE无关通路调节ICH后的神经元铁代谢。
STIM1 MUT显著降低了总铁含量,并改善了神经元细胞的存活率。STIM1 MUT显著减轻了脂质过氧化,还降低了MDA和ROS水平,同时提升了GPX4活性和GSH/GSSG比值。此外,STIM1 MUT挽救了与铁死亡相关的线粒体形态变化。综合来看,这些结果表明STIM1与TFR1的相互作用通过影响TFR1活性,调控了ICH后的神经元铁摄取和铁死亡。

STIM1抑制剂S-IN-1可抑制脑出血后神经元铁死亡并改善脑损伤
根据STIM1-TFR1复合物晶体结构的虚拟筛选鉴定出候选化合物SIN1S-IN-1,通过抑制STIM1与TFR1之间的相互作用,减轻ICH后神经元铁块死亡。接受S-IN-1治疗的ICH小鼠脑水肿程度减轻,存活神经元数量增加,血浆NSE水平降低。说明S-IN-1可以改善ICH小鼠的脑组织损伤和神经损伤,具有临床应用潜力。
总结
本研究强调了STIM1在促进神经元铁块凋亡和加重ICH后脑损伤中的关键作用。在机制上,STIM1在直接调节铁稳态方面具有独特的分子功能,该稳态通过与TFR1的相互作用促进铁的积累。STIM1-TFR1相互作用的特异性抑制剂S-IN-1,为抑制神经元铁剥蚀和改善脑损伤提供了有前景的治疗策略。这些发现有助于推进我们对ICH后神经元铁剥落的病理生理机制的理解,并为脑损伤治疗提供了有前景的靶点。
