前促胰液素(EREG)是表皮生长因子受体/EGFR和ERBB4的配体。能促进EGFR和ERBB4的酪氨酸磷酸化。通过调节血管生成和血管重塑以及刺激细胞增殖,参与炎症、伤口愈合、组织修复和卵母细胞成熟过程。
EREG的表达分布
EREG主要表达在淋巴和骨髓组织中,EREG主要表达在单核细胞中,在巨噬细胞中,霍夫鲍尔细胞,库普弗细胞树突状细胞,朗格汉斯细胞中都有少量表达。

(数据来源 uniprot)
EREG的结构和受体
EREG是一种单通道I型膜蛋白,由169个氨基酸组成,具有信号肽,N端胞外区,跨膜区和C端胞质区。胞外区具有表皮生长因子样结构域。
EREG首先合成一种分子量约为19kDa(未糖基化状态)的前体蛋白前表皮调节素(proepiregulin),经过糖基化修饰后形成约30kDa的跨膜蛋白。在整合素和金属蛋白酶的作用下,proepiregulin被切割释放出含有约46-50个氨基酸的成熟EREG多肽。
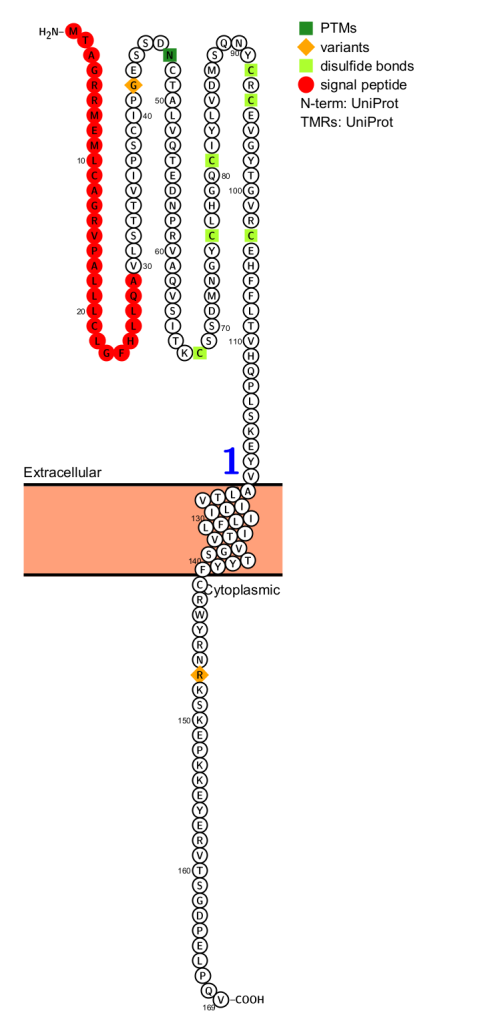
(数据来源 uniprot)
EREG的信号转导和在肿瘤微环境中的作用
可溶性EREG与EGFR(ERBB1)和ERBB4结合,诱导受体同源或异源二聚化。EREG通过结合EGFR(ERBB1/HER1)和ErbB4(HER4)激活下游信号通路,RAS/RAF/MEK/ERK通路,PI3K/AKT/mTOR通路,JAK/STAT通路。通过自分泌、旁分泌或近分泌方式作用于肿瘤细胞或TME中的其他细胞(如成纤维细胞、巨噬细胞)。

(数据来源 Wang C.Oncogene. 2022)
促进肿瘤发生与进展
自分泌和旁分泌EREG可能主要激活各种癌症TME中有助于肿瘤发生的EGFR下游途径。在结肠炎相关癌症中,基质来源的EREG通过ERK通路促进肠上皮细胞增殖。
EREG介导肿瘤转移
EREG通过JAK2/STAT3和IL-6信号诱导正常成纤维细胞向CAF转化,进而促进肿瘤细胞的EMT。EREG表达可能在结肠CSC中诱导,并与耐药性相关。在乳腺癌中,EREG是“肺转移签名”(LMS)基因之一,与MMP1/2、COX2协同促进肺转移。在头颈癌、唾液腺癌等模型中,EREG通过EGFR/ERK/AKT通路增强细胞迁移能力。
促进癌症干细胞(CSC)特性
CRC细胞中EREG表达增加,与癌症干细胞(CSC)特征相关,并在肿瘤进展过程中的转移中起关键作用。在结肠癌中,EREG在LGR5阳性和耐药LGR5阴性干细胞中均有表达,提示其在干细胞维持与耐药转换中发挥作用。在胶质瘤中,EREG表达与mRNA-based stemness index正相关,提示其促进肿瘤干细胞特性。
介导耐药性
EGFR-TKI耐药:在NSCLC中,肿瘤相关巨噬细胞(TAM)分泌的EREG通过EGFR/ERBB2/AKT通路诱导EGFR-TKI(如erlotinib)耐药。在结直肠癌中,EREG通过miR-215-5p/TYMS轴介导5-FU耐药。在乳腺癌中,EREG通过激活EGFR信号诱导tamoxifen耐药,并促进Warburg效应(有氧糖酵解)。
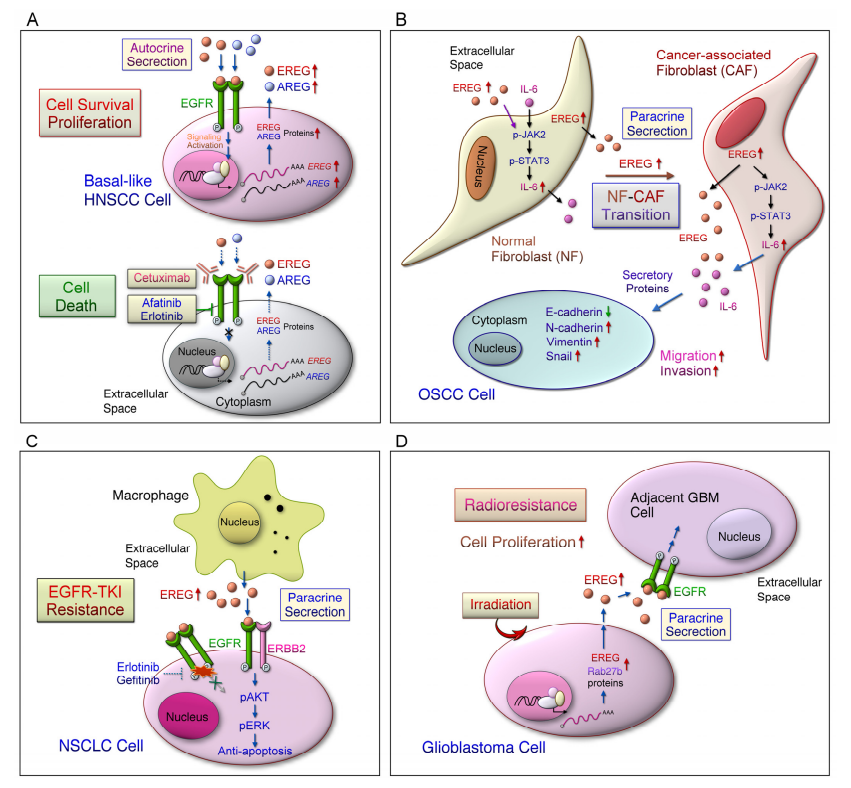
(数据来源 Cheng WL, et al. Int J Mol Sci. 2021)
EREG的靶向治疗
LY-3848575是礼来公司开发的一款靶向EREG的单克隆抗体,礼来公司正在进行一项名为“一项2期、随机、双盲、安慰剂对照、剂量探索研究,评估与远端感觉性多发性神经病相关的慢性神经性疼痛的LY3848575”的2期研究。该研究旨在评估LY3848575与安慰剂相比在治疗从脚部开始并向上发展到腿部的神经疼痛方面的安全性和有效性。
Fepixnebart(LY3016859)是礼来公司开发的一款针对TGFA和EREG的双特异性抗体。正在进行一项研究(NCT04529096)旨在测试LY3016859治疗骨关节炎疼痛的安全性和有效性。该试验是慢性疼痛主方案 H0P-MC-CPMP(NCT05986292)的一部分,该方案旨在加速慢性疼痛新疗法的开发。
我们收集整理一批EREG相关抗体序列信息。文档可关注公众号“迈思生物”,号内回复“ EREG ”下载。
