血小板衍生生长因子受体α(PDGFRA)又称为CD140a,是一种酪氨酸蛋白激酶(TK),作为PDGFA,PDGFB和PDGFC的细胞表面受体,在胚胎发育,细胞增殖,生存和趋化中起重要作用。大PDGFRα被认为是转移性肿瘤生长、血管生成和扩散的重要因素。它作为酪氨酸激酶抑制剂的靶点,被开发用于治疗各种恶性肿瘤。
PDGFRA的表达分布
PDGFRA主要表达在间质细胞,莱迪希细胞,胶质细胞,成纤维细胞,星状细胞中。约10-15%的胃肠道间质瘤(GIST)中发生PDGFRA突变引起的,它还在胶质母细胞瘤等脑肿,瘤横纹肌样瘤、甲状腺癌中表达。

(数据来源 uniprot)

(数据来源 uniprot)
PDGFRA的结构
PDGFRA是一种 I 型跨膜蛋白,这些受体的特征包括一个糖基化胞外结构域(由与配体结合的5个免疫球蛋白样模块组成)、一个螺旋跨膜结构域和一个具有酪氨酸激酶活性的胞内区域。当配体(如PDGF)与两个PDGFRA受体结合时,会导致两个受体二聚化(通常是PDGFRA-PDGFRA同源二聚体或PDGFRA-PDGFRB异源二聚体)。
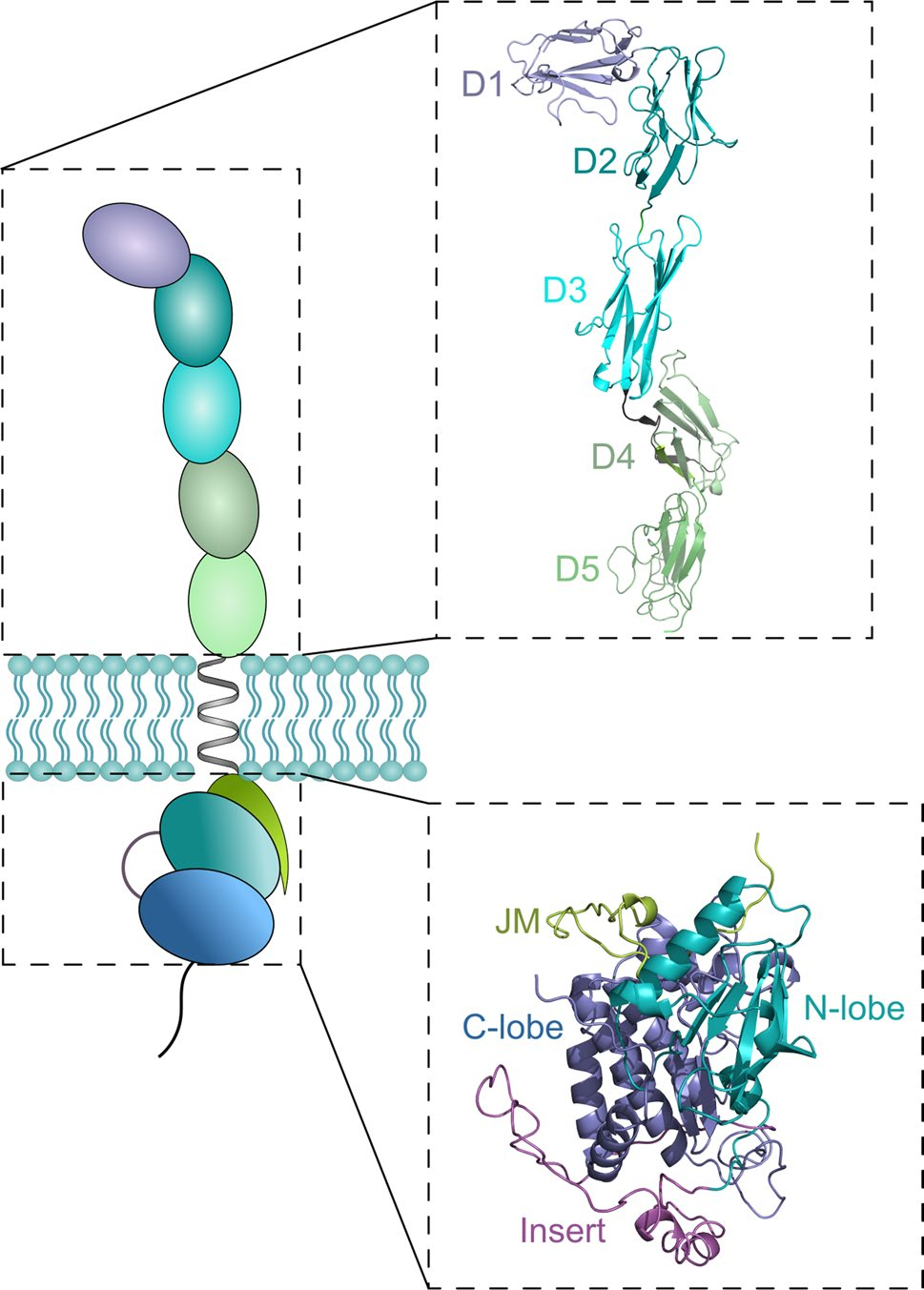
(数据来源 Guérit E, Cell Mol Life Sci. 2021)

(数据来源 Sun Y, et al. Front Oncol. 2022)
PDGFRA的信号通路和在肿瘤中的作用
PDGFR与PDGF配体结合后启动二聚化和磷酸化,从而激活各种下游信号通路,如PI3K/AKT/PKB通路、MAPK/ERK通路、JAK信号转导和STAT途径,Notch途径。
PDGFRA主要在癌细胞中表达,而PDGFRB则在基质细胞和血管周围细胞中发现,PDGFRA表达增加与神经胶质瘤的癌症进展呈正相关。恶性肿瘤细胞经常具有PDGFRA突变,这会导致某些癌症中PDGFRA下游信号通路的慢性激活,例如胃肠道间质瘤(胃肠道间质瘤)。在一些肿瘤中,PDGFs通过各种细胞和分子改变刺激肿瘤生长,如肿瘤微环境中的旁分泌信号,促进EMT和血管生成。
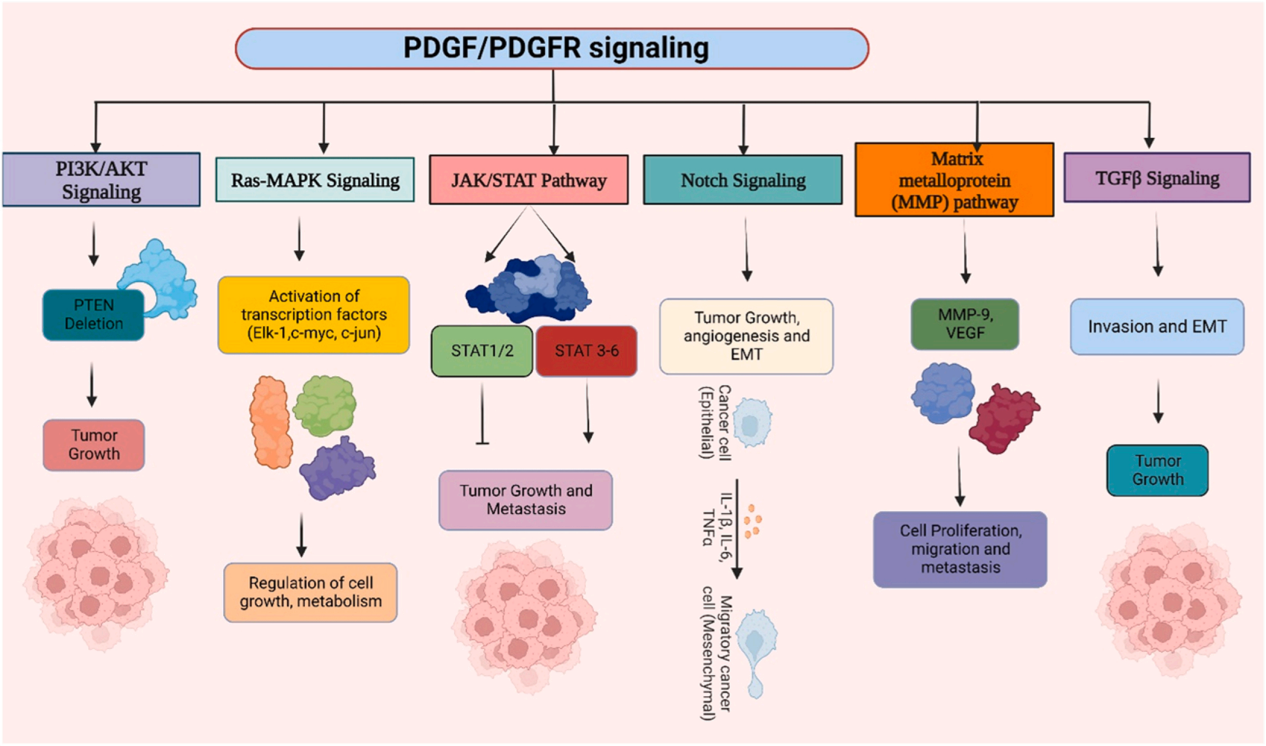
(数据来源 Pandey P, et al. Biomed Pharmacother. 2023)
PDGFRA的靶向治疗
由于抑制PDGFR可抑制癌症增殖、转移、侵袭和血管生成,并提高抗癌药物的抗肿瘤效果。基于PDGFR通路的癌症治疗出现了一些新的治疗策略。
Olaratumab(IMC-3G3)是一种靶向PDGFRA的单克隆抗体,它通过与PDGFRα特异性相互作用发挥作用,防止PDGF配体结合(PDGF-AA、PDGF-CC和PDGF-BB)、抑制PDGFR激活并阻断下游信号传导。在许多肿瘤模型中,Olaratumab下调细胞增殖。基于一项晚期软组织肉瘤的Ib/II期研究结果,于2016年10月在美国首次获得全球批准用于软组织肉瘤的治疗。在这项研究中,Olaratumab联合doxorubicin治疗显示,与doxorubicin单独治疗相比,Olaratumab单抗联合doxorubicin治疗显著延长了11.8个月的中位总生存期。欧洲药品管理局(2016)临时批准其用于治疗不适合手术或放疗的转移性软组织肉瘤患者。目前正在国外进行治疗软组织肉瘤的确证性III期临床试验(NCT02451943)。

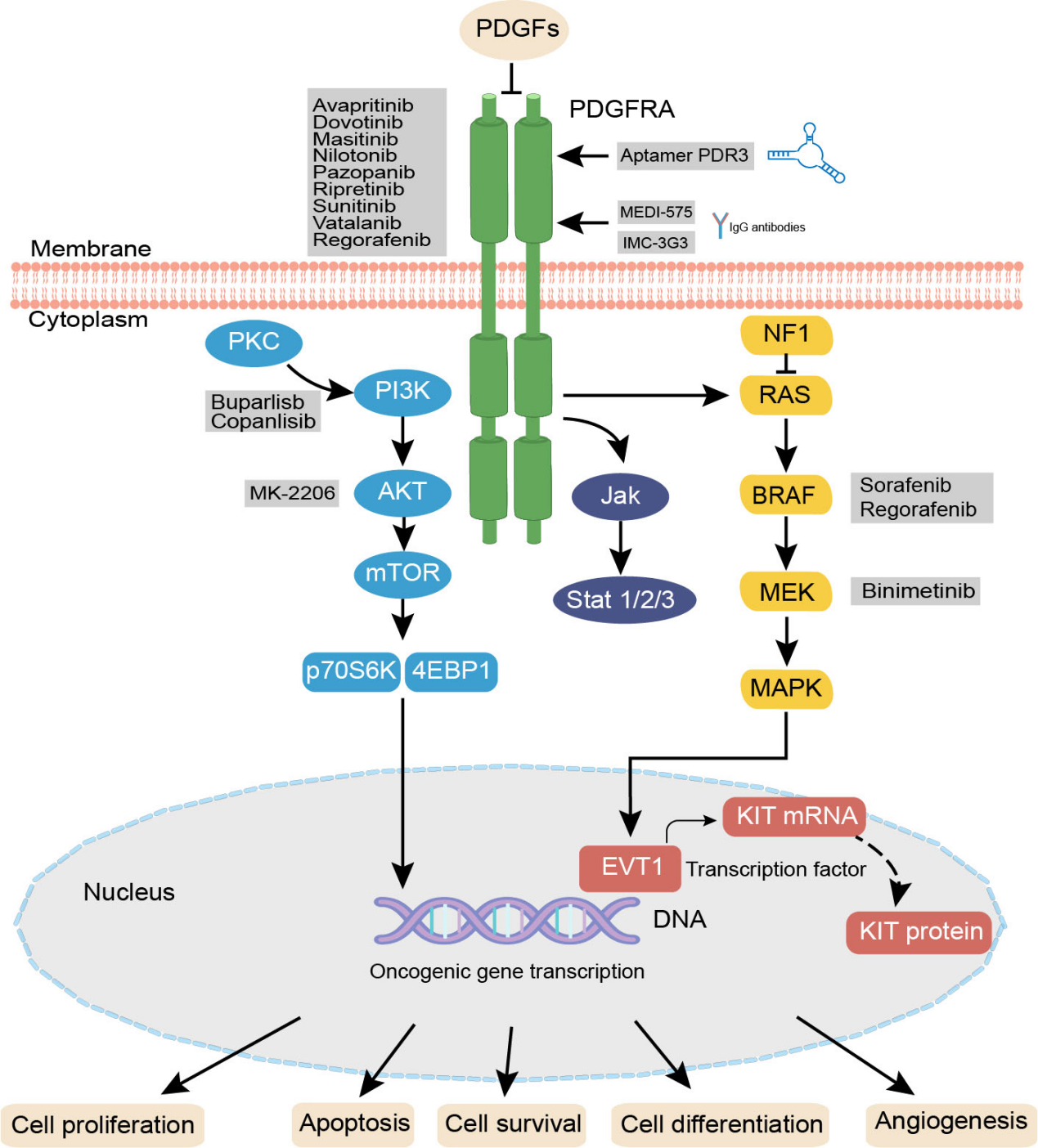
(数据来源 Sun Y, et al. Front Oncol. 2022)
我们收集整理一批PDGFRA相关抗体序列信息。文档可关注公众号,号内回复“PDGFRA”下载。
