血小板糖蛋白VI(GPVI)是一种胶原受体,参与胶原诱导的血小板粘附和活化在血小板促凝活性及随后凝血酶和纤维蛋白形成中起关键作用。这种促凝功能可能促进动脉和静脉血栓形成。该信号通路涉及FcRγ链、Src激酶(可能为FYN或LYN)和SYK、衔接蛋白LAT,并导致PLCG2的激活。它是动脉血栓并发症的治疗靶点。
GP6的表达分布
GP6主要表达在血小板,肾单位细胞,导管细胞,神经元细胞中,在单核吞噬细胞,NK细胞,T细胞中有少量表达。
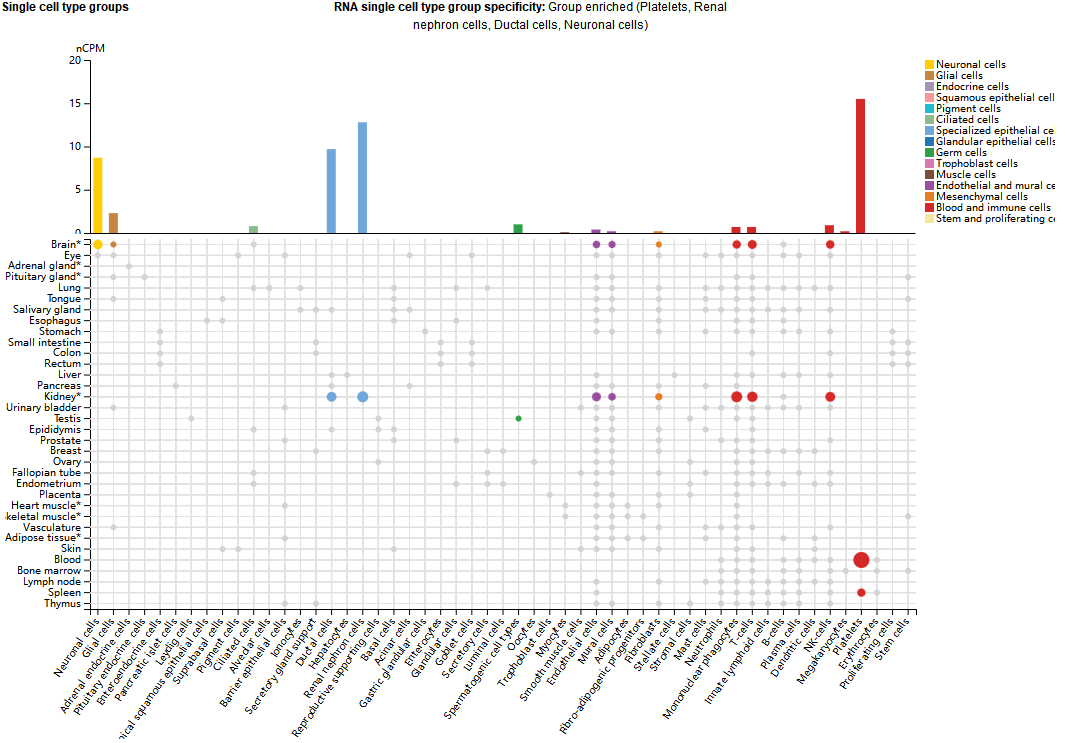
(数据来源 uniprot)
GP6的结构和信号转导调控
GP6是一种I型跨膜蛋白,由339个氨基酸组成,它包括胞外Ig样结构域、D1和D2、一个糖基化柄、单个跨膜区和短胞内尾细胞质尾部具有富含脯氨酸的区域,该区域与非受体酪氨酸激酶的Src同源3结构域结合。GPVI通过其细胞外D1结构域结合胶原蛋白。GPVI的功能形式一般以单体形式存在,D2结构域会引起其二聚化。
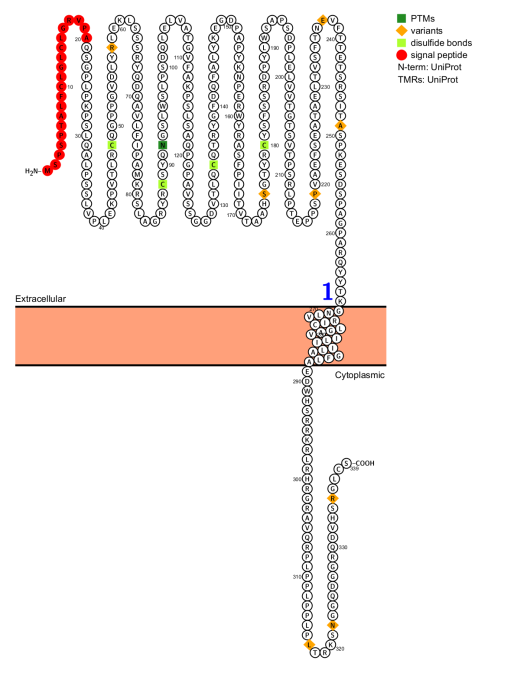
(数据来源 protter)
GPVI通过跨膜区域形成的盐桥和细胞内尾部内的相互作用与膜中的FcR-γ链形成复合物。FcR-γ链是同型二聚体,每个链含有免疫受体酪氨酸激活基序(ITAM)。交联GPVI诱导保守的ITAM酪氨酸残基被Src家族激酶(sfk)Fyn、Lyn和Src磷酸化。将Syk募集到磷酸化的ITAM启动下游信号传导,导致PLCγ2活化和血小板聚集。

(数据来源 Li R, et al. Drug Discov Today. 2025)
GP6在血栓形成中的作用
GPVI活性通过二聚化和受体聚集两种机制进行调节,以有效激活血小板。血小板表达多种胶原蛋白受体。血流条件下血管损伤后,GPIbα-血管性血友病因子(VWF)、整合素α2β1-胶原和GPVI-胶原的相互作用共同介导血小板粘附。其中,GPIbα-VWF在高剪切应力虽然不是必需的,但整合素α2β1可以稳定胶原蛋白结合并促进GPVI二聚化和聚集,从而放大GPVI激活并协同支持血小板聚集和血栓形成。作为胶原蛋白的中心受体,GPVI激活FcRγ链依赖性途径,引发钙流和整合素αIIbβ3激活,促进血小板牢固粘附和血栓形成。此外,在极高的剪切应力,GPVI和纤维蛋白之间的相互作用对血栓稳定性有显著贡献。GPVI通过促进血小板聚集和凝血在血栓形成中发挥双重作用。
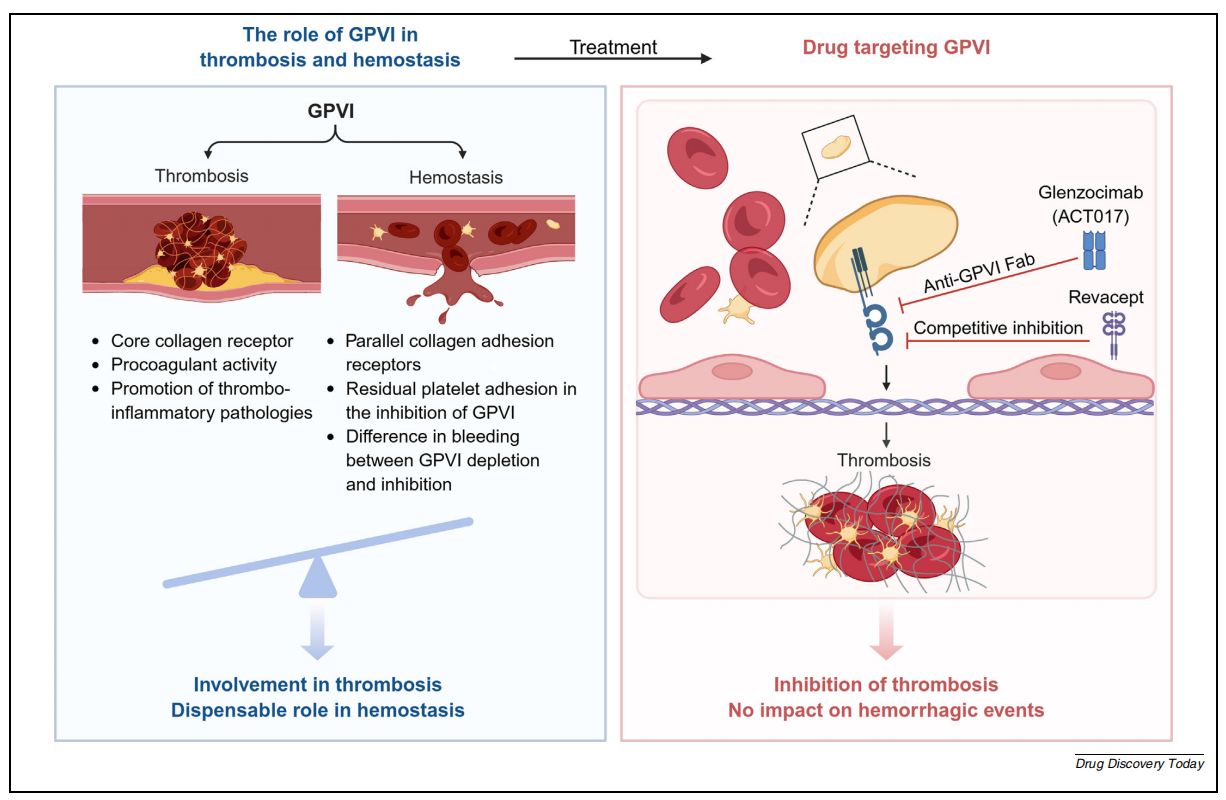
(数据来源 Li R, et al. Drug Discov Today. 2025)
GP6的靶向治疗
针对GP6的靶向治疗方式主要有glenzocimab抗体和Revacept融合蛋白。Glenzocimab(ACT017)是根据鼠单克隆抗体设计的人源化Fab片段,他主要用于治疗急性缺血性卒中肺栓塞。体外使用人类血小板的研究证明了其对胶原蛋白诱导的血小板聚集的有效抑制作用。Glenzocimab与GPVI的D2结构域结合,并阻断二聚化和配体结合。这导致受体聚集的有效抑制。
Revacept是一种Fc融合蛋白,它是通过将人GPVI的胞外结构域与人Fc结构域融合而产生的,形成具有特定铰链区的150 kDa同二聚体。模拟细胞外GPVI并与膜结合GPVI竞争配体结合。GPVI-Fc能有效抑制血小板与固定胶原蛋白的粘附和血栓形成。在小鼠颈动脉损伤模型中,给予 1-2 mg/kg剂量的GPVI-Fc可减少牢固的血小板粘附和聚集。在一项I期临床试验中,研究人员在30名健康男性受试者中评估了Revacept的安全性、耐受性和PK/PD。安全性评估显示,Revacept没有显着延长出血时间,对血小板计数或凝血参数没有影响,也没有检测到抗药物抗体。此外,在研究期间没有观察到严重的不良事件。
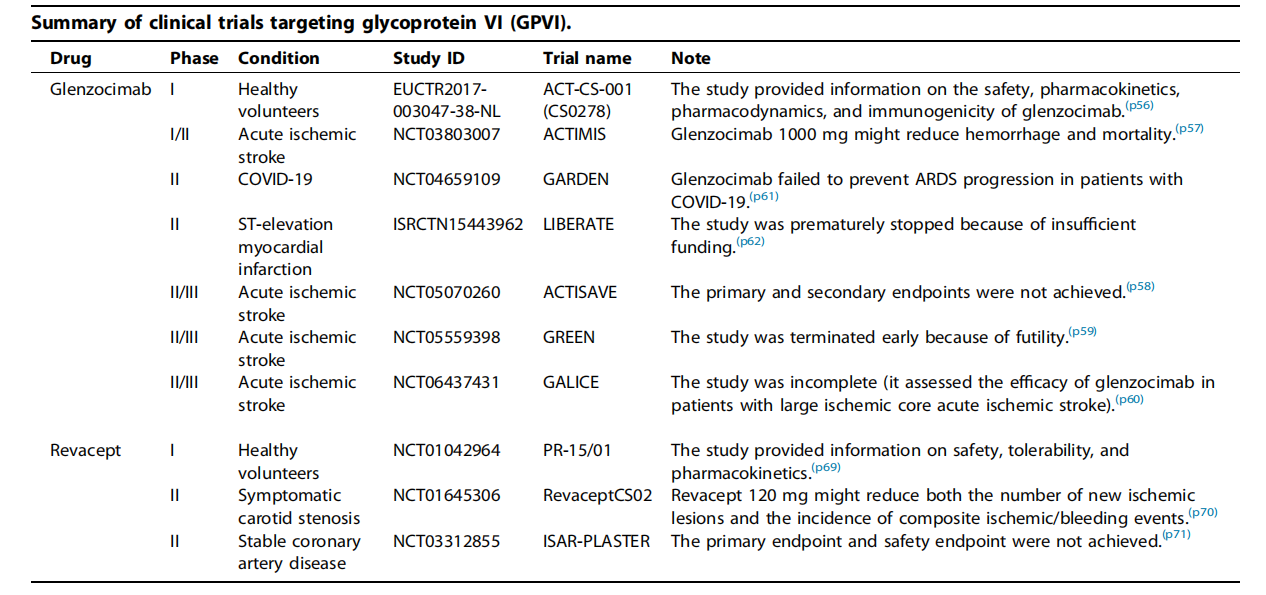
(数据来源 Li R, et al. Drug Discov Today. 2025)

除此之外,还有其他方法可以抑制GPVI信号通路,GPVI信号传导需要SFKs和FcR-γ链相互作用到GPVI的细胞内尾部。SFKs在GPVI激活时磷酸化FcR-γ链的ITAM酪氨酸残基,这导致进一步的下游信号传导。阻断GPVI与SFKs或FcR-γ链的相互作用将导致信号抑制。GPVI在跨膜区之前被ADAM10切割,这一过程称为脱落。胞外GPVI从血小板表面释放,留下由跨膜区和胞内区组成的截短GPVI。由于不能被配体聚集,这种裂解结构不再具有信号活性。ADAM10诱导的脱落由Tspan5和33介导。SFKs在GPVI激活时磷酸化FcR-γ链的ITAM序列。这会诱导下游信号传导事件。G6b-B与GPVI和细胞内磷酸酶SHP2结合。使SHP2与FcR-γ链接近可促进ITAM序列的去磷酸化并抑制进一步的下游信号传导。

(数据来源 Slater A, et al. Eur Heart J Cardiovasc Pharmacother. 2024)
我们收集整理一批GP6相关抗体序列信息。文档可关注公众号“迈思生物”,号内回复“GP6 ”下载。
