成纤维细胞生长因子受体(Fibroblast growth factor receptor 1,FGFR1)是FGFR家族成员,是一种跨膜蛋白,属于受体酪氨酸激酶。它在细胞增殖、分化、迁移和存活等关键生物学过程中扮演核心角色,尤其在胚胎发育、血管生成和组织修复中至关重要。FGFR1的异常活化(如突变、扩增或易位)与多种癌症(如乳腺癌、肺癌、膀胱癌)和发育性疾病密切相关。
FGFR1的表达分布
FGFR1主要表达在星形细胞瘤、神经母细胞瘤和肾上腺皮质细胞系中。一些异构体也在包皮成纤维细胞系中被检测到,然而异构体17、异构体18和异构体19在这些细胞中却未能检测到表达。
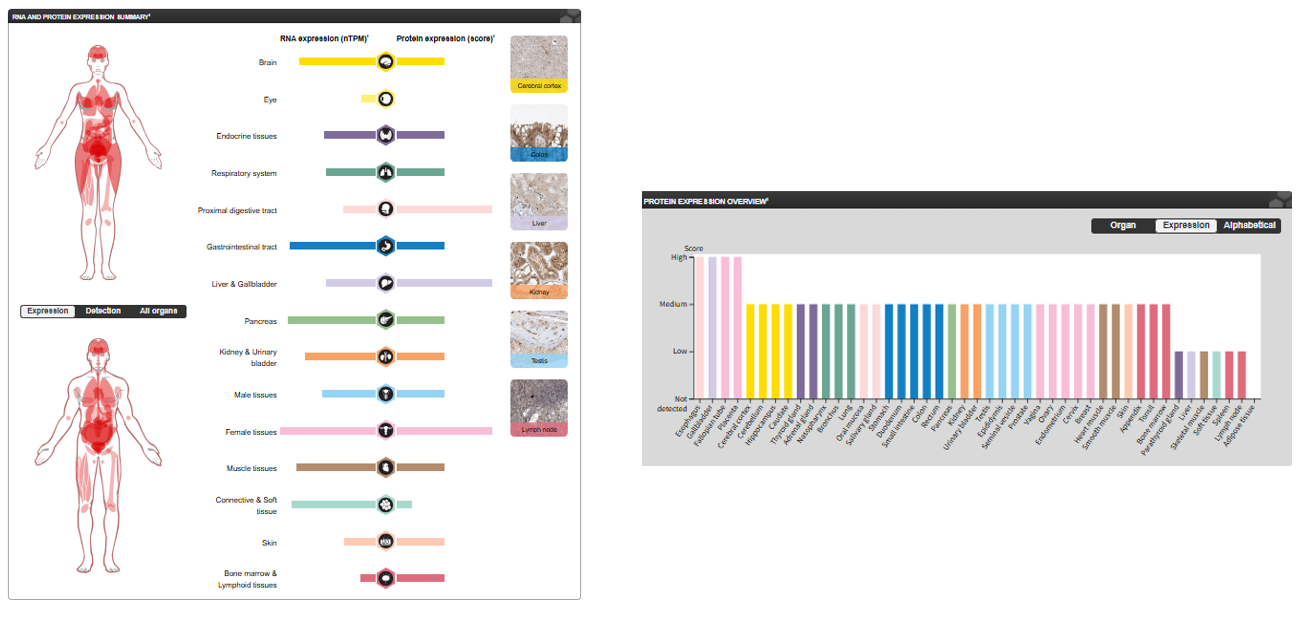
(数据来源 uniprot)
FGFR1的结构
FGFR1是由FGFR1基因编码的长度为822 aa,分子量约91.8 kDa的Ⅰ型跨膜蛋白,由多个高度保守的结构域组成,从细胞外到细胞内可分为三个主要部分。
胞外区(22-376 aa):这是FGFR1识别并结合配体(FGFs)的部分,由三个免疫球蛋白样结构域(Ig-like domains,简称D1, D2, D3)组成。D1域:最远端的结构域,与一个酸性盒(acid box)区域相连,被认为在稳定受体非活性状态和防止自发二聚化中起作用。D2域和D3域:这是配体结合的核心区域。D2和D3之间的区域决定了FGFR1对特定FGF配体的结合特异性。“酸盒”区域:位于D1和D2之间,富含酸性氨基酸,其功能是自抑制,在没有配体时帮助维持受体的非活性状态。
跨膜区(377-397 aa):由一个α螺旋组成,其主要功能是将受体锚定在细胞膜上,并将胞外区的构象变化传递到胞内区。
胞质区(398-822 aa):位于细胞膜内侧,含有关键的酪氨酸残基,在受体激活前的自抑制中起作用。a)酪氨酸激酶结构域(TK域):这是FGFR1的催化核心和功能中心。它能够利用ATP将磷酸基团转移到特定靶蛋白的酪氨酸残基上,从而启动下游信号通路。该结构域在FGFR家族中高度保守。b)C端尾部:包含多个可被自身磷酸化的酪氨酸残基,这些位点磷酸化后,可作为下游信号蛋白(如PLCγ, FRS2)的停靠位点(docking sites),是募集和激活下游信号分子的关键。
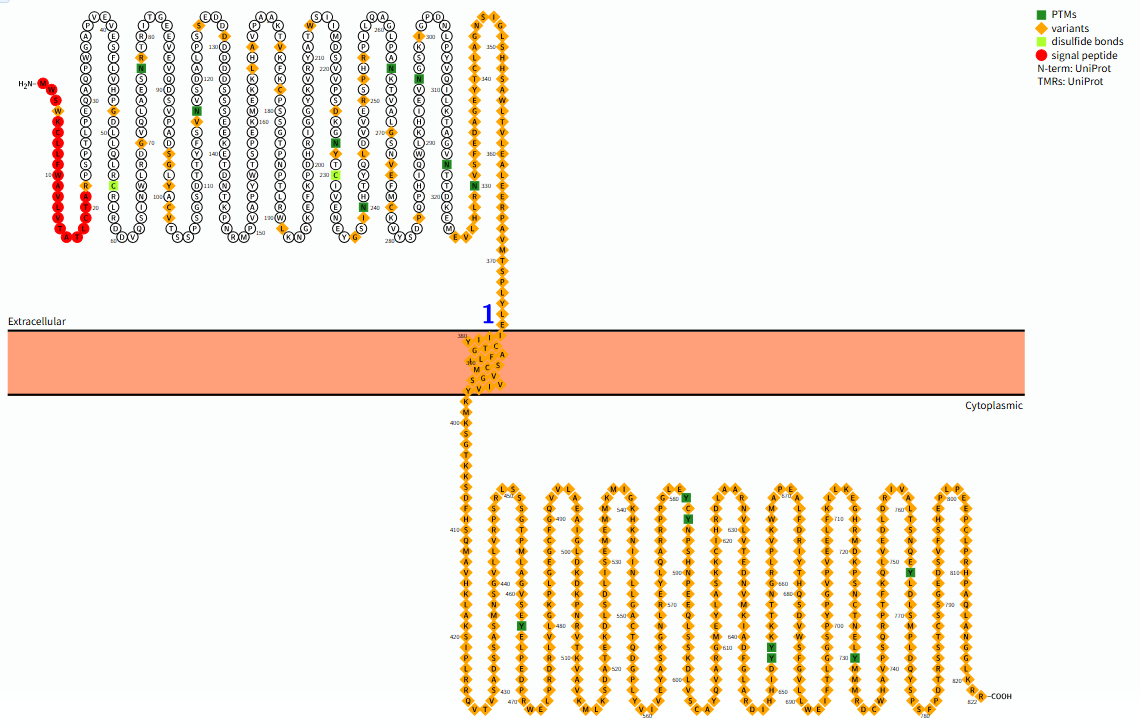
(数据来源:protter)
FGFR1的信号通路
a)RAS-MAPK通路:路径 “FRS2α→GRB2→SOS→ RAS →RAF→MEK→ERK”,这是FGFR1最经典的通路。活化的ERK进入细胞核,磷酸化转录因子(如c-Fos, c-Jun),主要调控细胞增殖和分化。
b)PI3K-AKT通路:通过FRS2α或磷酸化的FGFR直接募集PI3K→PIP2转化为PIP3→ AKT 激活,AKT是核心节点,调控细胞存活(抑制凋亡)、代谢和增殖。
c) PLCγ通路:PLCγ直接被募集到受体并激活→水解PIP2生成IP3和DAG→IP3促使胞内钙离子释放,DAG激活PKC,最终调控细胞迁移、增殖和分化。
d)JAK-STAT通路:在某些情况下,激活的FGFR1可以磷酸化并激活STAT蛋白,STAT形成二聚体进入细胞核,最终调控基因表达和细胞命运。
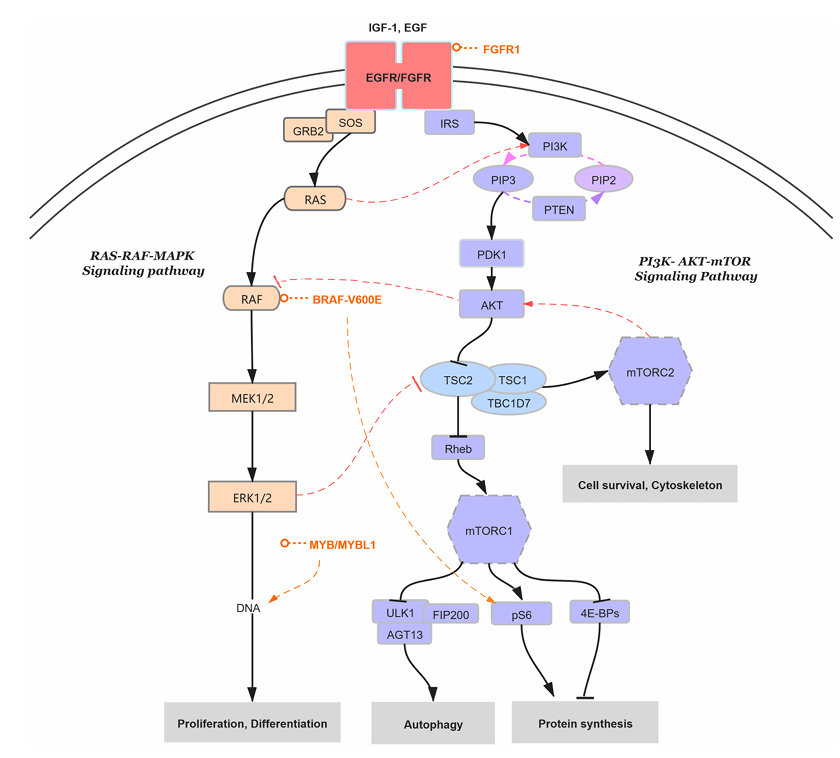
(数据来源:Xie M, et al. Front Neurosci. 2023)
FGFR1与疾病
非酒精性脂肪性肝病(non-alcoholic fatty liver disease,NAFLD): 当机体处于高脂等异常状态时,游离脂肪酸(Fatty Acids)积累,会抑制FGF21通路,引发一系列促NAFLD反应:a)脂质合成(Lipogenesis)增强:SREBP1、PPARγ、FAS等脂质合成相关蛋白活跃,肝脏脂肪堆积;b)炎症反应(Inflammation)激活:IL-1β、MCP-1、TNF-α等炎症因子释放,加重肝脏损伤,最终推动NAFLD发生。萝卜硫素(Sulforaphane)可通过激活FGF21→FGFR1+β-Klotho复合物信号通路,扭转病理过程,改善脂质代谢(促进脂肪分解和增强脂肪酸氧化),通过p38信号通路,进一步强化代谢调节,最终实现NAFLD保护。
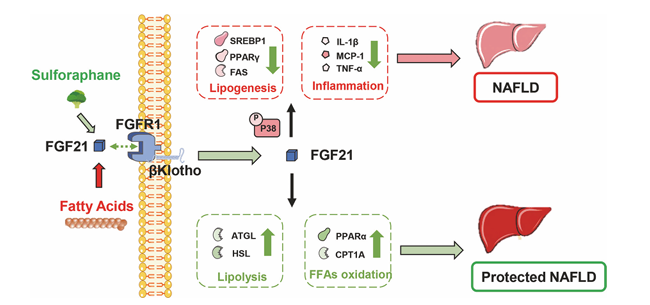
(数据来源:Desale SE, et al. Mol Biomed. 2021)
前列腺癌(prostate cancer ):转铁蛋白(TF)结合Fe3+,通过细胞膜上的转铁蛋白受体1(TFR1)进入细胞,释放Fe2+,形成不稳定铁池(LIP)。LIP是癌细胞摄取铁的关键形式,TFR1过表达会增加LIP,而FGFR1能够通过抑制E3泛素连接酶FBXL5,稳定铁调节蛋白IRP2;IRP2上调转铁蛋白受体TFR1的表达,促进铁摄取并形成不稳定铁池(LIP);LIP进一步通过激活c-Myc正反馈增强TFR1表达,导致铁持续积累,最终驱动肿瘤增殖与恶性进展。
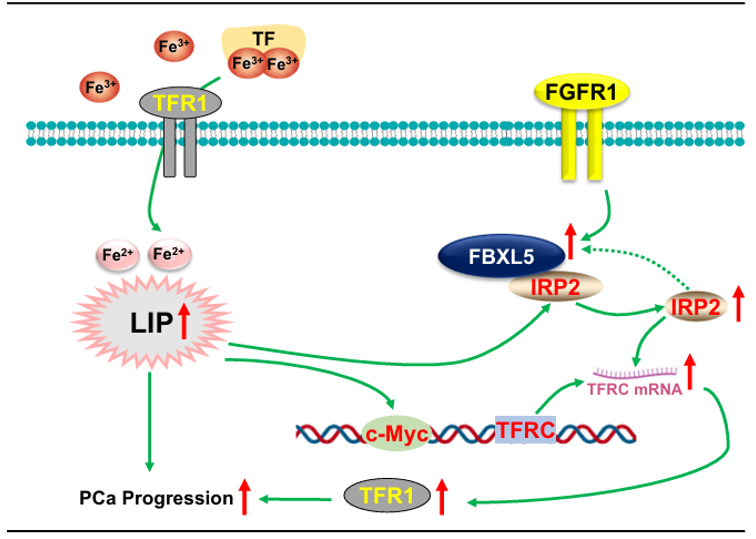
(数据来源:Lin H, et al. Commun Biol. 2024)
乳腺癌(Breast Cancer)领域:FGFR可以通过FGFR-MEK-ERK-c-FOS-FOXQ1信号通路,促乳腺癌生长。通过膜结合型FGFR1(mFGFR1)或经人工诱导聚合与豆蔻酰化修饰的胞内型FGFR1(iFGFR1)激活,引发磷酸化并启动下游MEK-ERK信号传导。活化的ERK2进入细胞核,磷酸化转录因子c-FOS,使其结合于FOXQ1基因启动子区域,促进FOXQ1转录。高表达的FOXQ1进而驱动肿瘤细胞增殖、集落形成及体内生长。
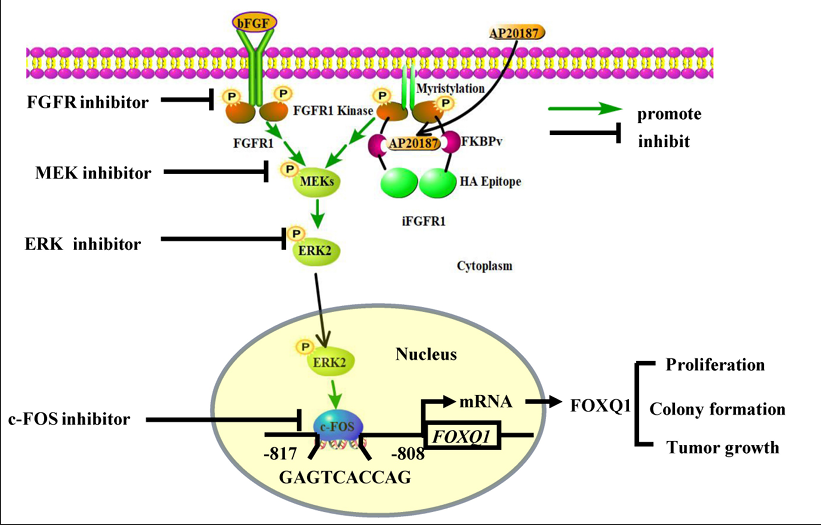
(数据来源:Lin Y, et al. Int J Biol Sci. 2023)
FGFR1的靶向治疗
M-6123是由Merck KGaA&Ligand Pharmaceuticals&NGM Biopharmaceuticals联合研发的一款靶向FGFR1的单克隆抗体药物。其主要的作用机制是作为FGFR1的拮抗剂,特异性结合FGFR1,抑制其下游信号传导,用于治疗肺癌和间皮组织肿瘤。目前处于临床前阶段。
NGM-313是由NGM Biopharmaceuticals研发的一款靶向FGFR1和KLB的单克隆抗体药物。其主要的作用机制是作为FGFR1的刺激剂和KLB的激动剂,靶向FGFR1/KLB复合体,刺激β-Klotho(KLB)依赖性信号传导,用于治疗代谢功能障碍的脂肪肝病。于2020年11月11日,批准临床二期试验,但目前已经终止。
OM-RCA-001是由Goodwin Biotechnology研发的一款靶向FGFR1的单克隆抗体药物。其主要的作用机制作为FGFR1的拮抗剂,通过拮抗FGFR1活性抑制肿瘤生长,用于治疗肾肿瘤。目前处于药物发现阶段。
VHH agonist是由Epsilon Molecular Engineer研发的一款靶向FGFR1的单克隆抗体药物。其主要的作用机制是作为FGFR1的刺激剂,采用纳米抗体(VHH)技术激活FGFR1,具体适应症暂无。目前处于药物发现阶段。
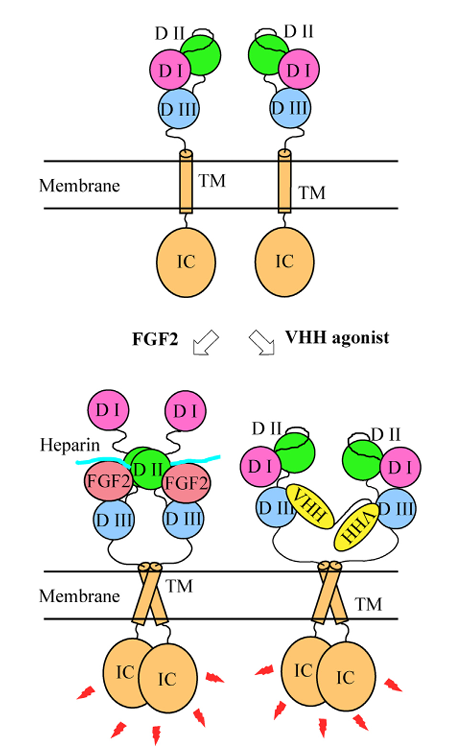
(数据来源:Ryo Yonehara, et al. J Biol Chem. 2023)
我们收集整理一批FGFR1相关抗体序列信息。文档可关注公众号“迈思生物”,号内回复“ FGFR1 ”下载。
