B7H4是含V-set结构域的T细胞活化抑制剂1(VTCN1),也称为B7x,是B7家族的成员,是一种抑制性免疫检查点。它通过抑制T细胞的活化、增殖、细胞因子的产生和细胞毒性的发展负调控T细胞介导的免疫应答。当表达于肿瘤巨噬细胞表面时,与调节性T细胞(Treg)一起在抑制肿瘤相关抗原特异性T细胞免疫中发挥重要作用。
B7H4的表达分布
B7H4主要表达在导管细胞、腺腔细胞、分泌细胞、黏液腺细胞、乳腺腺细胞、集合管细胞、唾液腺管细胞中。
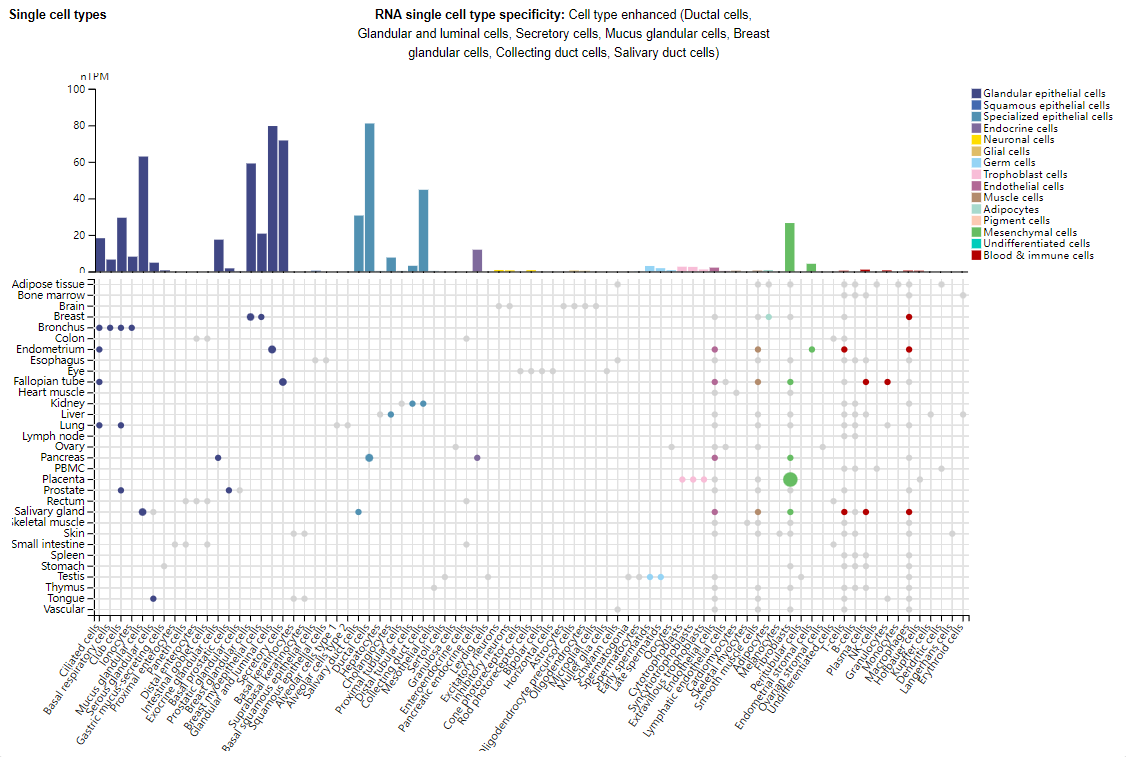
(数据来源 uniprot)
B7H4的结构
B7H4基因位于1号染色体的p12–13.1上。B7H4是一种I型跨膜蛋白,由282个氨基酸,包含一个信号肽、胞外结构、一个连续的茎区域,一个跨膜结构域和一个非常短的不带有信号基序的细胞质尾部。B7x的胞外域由1个Ig 可变(IgV)结构域和1个Ig恒定(IgC)结构域组成,与其他B7家族配体类似。B7x IgV采用由背面(AA 'BED股)和正面(CC 'C ' FG股)组成的β夹心折叠,其由B股和F股之间形成的二硫键稳定。
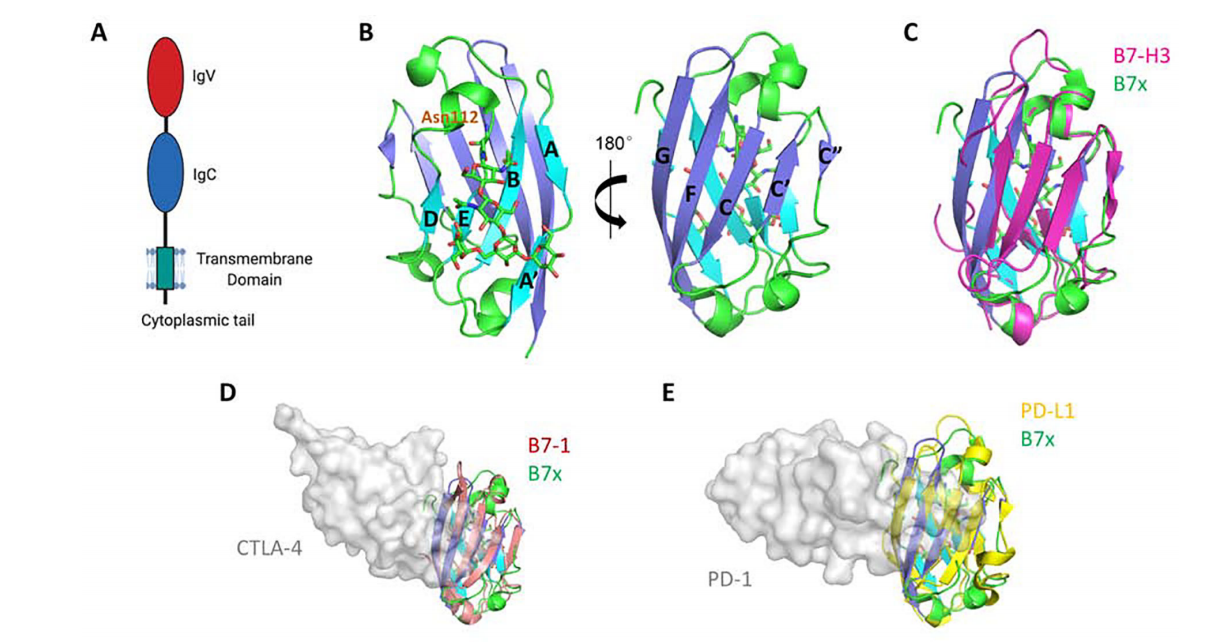
(数据来源 John P, et al. Trends Pharmacol Sci. 2019)
B7H4的功能
B7x通过调节T细胞功能介导多种免疫抑制机制。 B7x阻断效应CD4和CD8 T细胞的炎症功能,减少IFNγ等细胞因子的产生,并抑制其增殖。相反,B7x促进Treg功能,包括分泌IL-10等免疫抑制因子。B7x还调节T细胞的分化,抑制其极化为效应T细胞并抑制分化为Tregs。
B7x在多种癌症类型表达,例如,卵巢癌,乳腺癌,子宫内膜癌等。肿瘤表达的B7x与晚期疾病进展和较差的预后相关。B7x由肿瘤细胞和肿瘤相关巨噬细胞表达,介导肿瘤的免疫逃逸。肿瘤细胞表达的B7x会抑制抗肿瘤T细胞的活性,并促进这些T细胞进入衰竭、功能失调的状态。此外,B7x还能促进肿瘤相关中性粒细胞(骨髓源性抑制细胞)。在卵巢癌和神经胶质瘤中,肿瘤细胞分泌IL-6和IL-10等细胞因子,驱动肿瘤相关巨噬细胞中B7x的表达。
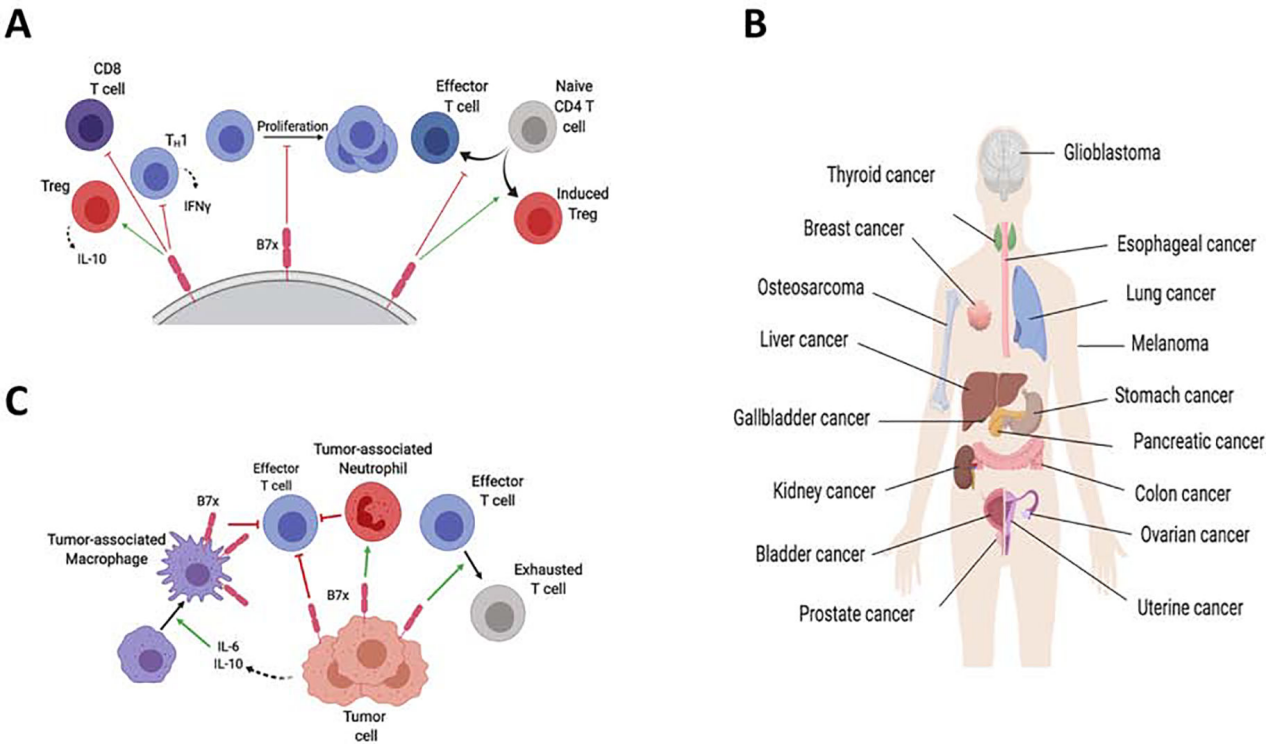
(数据来源 John P, et al. Trends Pharmacol Sci. 2019)
B7H4的靶向治疗
在卵巢癌(OC)和其他癌症中中针对B7-H4的免疫疗法的重点围绕ICI、过继细胞疗法(ACT)和抗体药物偶联物(ADC),双特异性抗体,有许多药物在临床开发中。
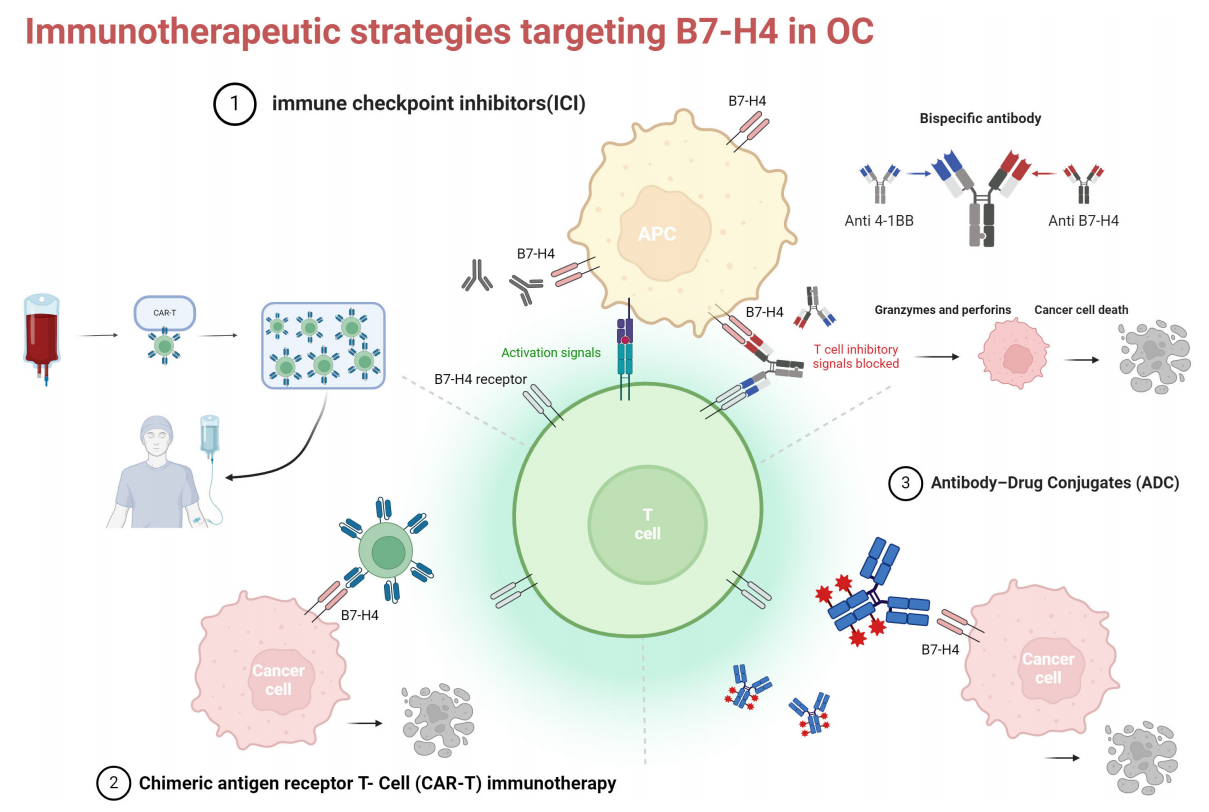
(数据来源 Zhou L, et al. Front Immunol. 2024)
HS-20089是上海翰森生物开发的一款靶向B7H4的抗体药物偶联物,目前处于临床2期研究阶段。HS-20089在OC中表现出良好的抗肿瘤活性,在铂耐药卵巢癌(PROC)中,客观缓解率(ORR)为66.7%,疾病控制率(DCR)为100%。
ABL103这是一种新型T细胞参与双特异性抗体,旨在同时靶向B7-H4和4-1BB。ABL103通过双重机制发挥作用,通过抑制B7-H4同时激活4-1BB来增强T细胞功能。这种新方法通过OC的TME中B7-H4依赖性4-1BB激活实现了强大的体外和体内抗肿瘤活性,并具有良好的安全性。
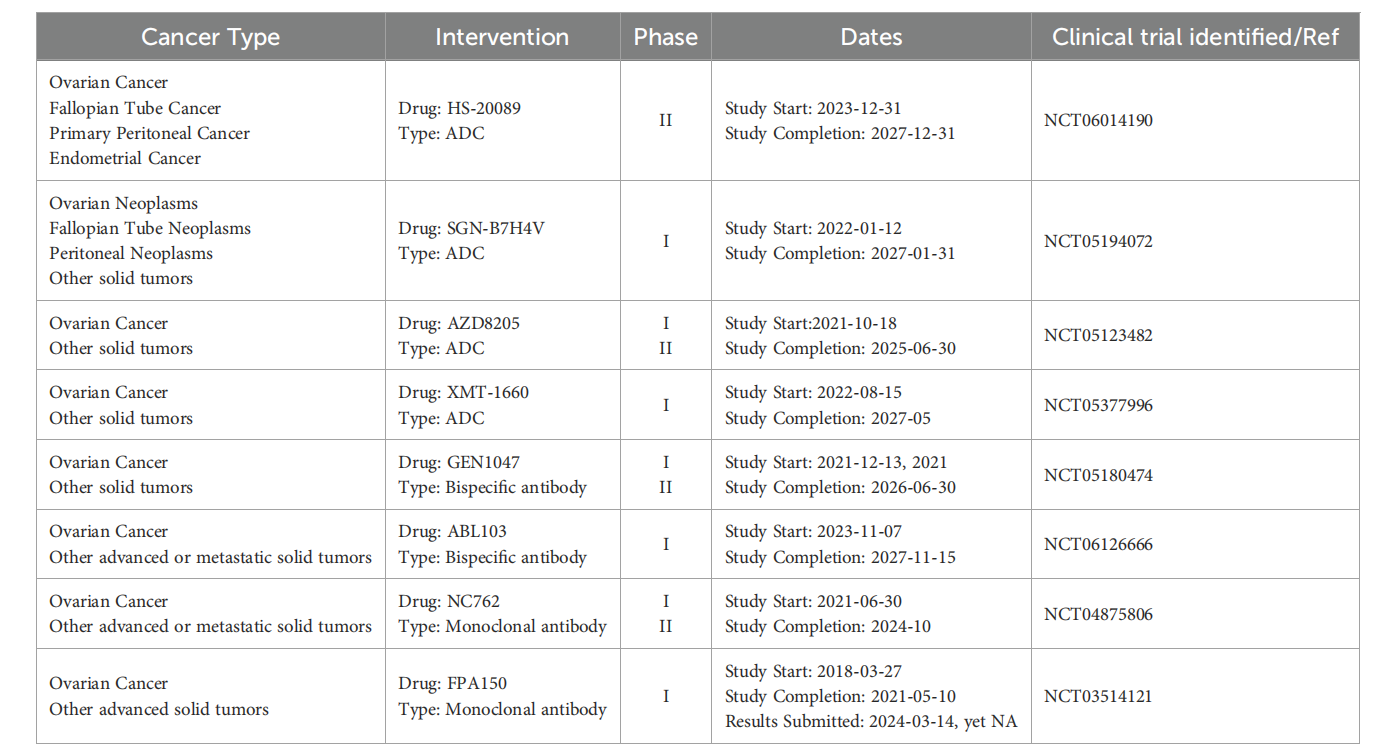
(数据来源 Zhou L, et al. Front Immunol. 2024)
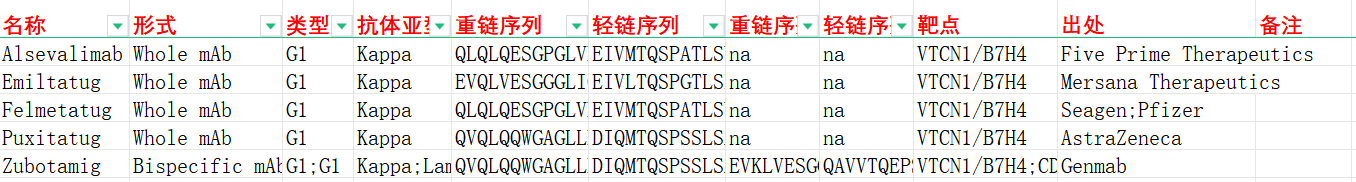
我们收集整理一批B7H4相关抗体序列信息。文档可关注公众号“迈思生物”,号内回复“B7H4 ”下载。