微管相关蛋白(Microtubule-Associated Protein Tau,MAPT)基因编码的Tau蛋白在神经元中主要功能是稳定微管,促进微管组装。在病理条件下,Tau蛋白会发生过度磷酸化,导致其从微管解离,形成细胞内的不溶性聚集体,这些聚集体被认为与多种神经退行性疾病的发病机制密切相关。
MAPT的表达分布
MAPT主要在神经元中表达。PNS-tau异构体在周围神经系统中表达,而其他异构体则在中枢神经系统中表达。
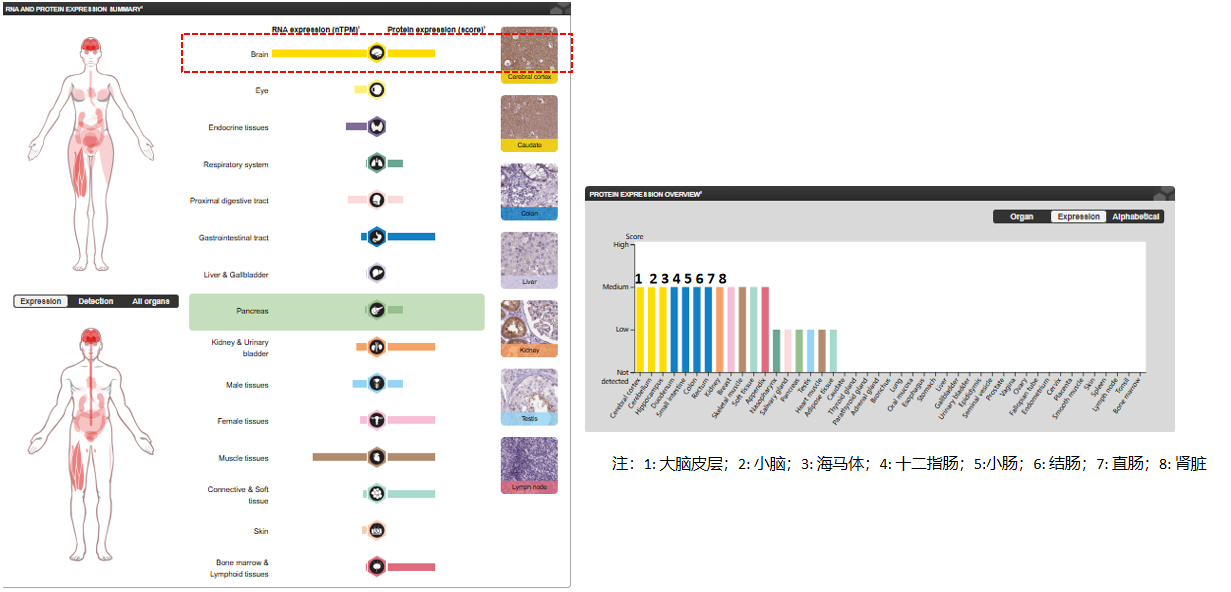
(数据来源 uniprot)
MAPT的结构
MAPT是由MAPT基因编码的长度为758 AA,分子量约78.9 kDa的一种神经元微管蛋白。MAPT通过可变剪接产生6种Tau亚型,在神经元中主导微管稳定和轴突运输。其结构域中MTBR决定微管结合能力,而N端和磷酸化位点调控互作与病理聚集。其结构域可分为以下几个部分:
N端投射域:位于氨基酸1-150aa区域,负责与细胞骨架蛋白互作,参与信号传导;
脯氨酸富集区:相邻于微管结合域,负责调控蛋白激酶(如GSK-3β、CDK5)的磷酸化位点;
微管结合域(MTBR):位于C端(含3-4个重复序列:R1-R4),负责结合微管;外显子10剪接决定3R/4R类型,4R亚型结合力更强。
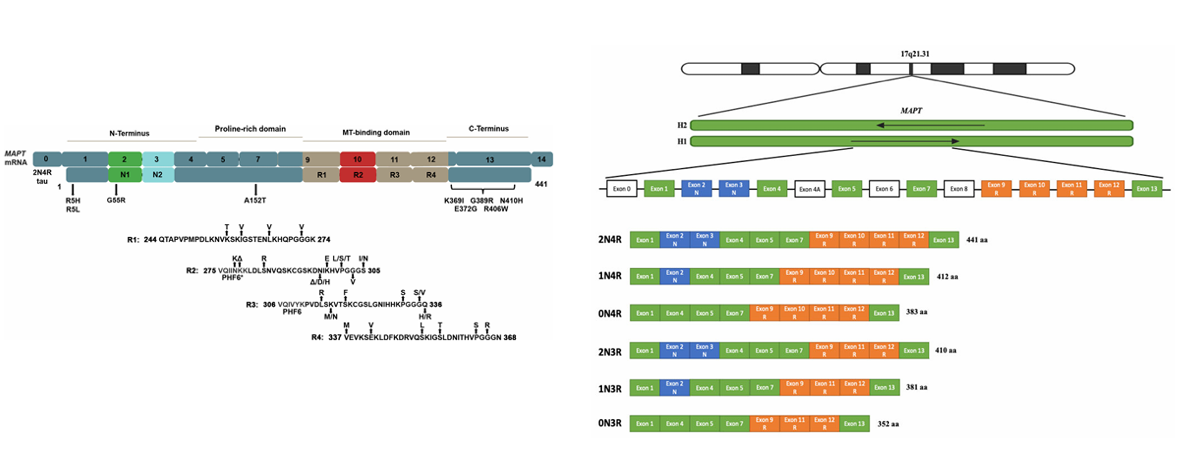
(数据来源 左:Strang KH, et al. Lab Invest. 2019;右:Leveille E, et al. Parkinsonism Relat Disord.2021)
MAPT的信号通路
Tau聚集抑制自噬:Tau蛋白异常聚集(如过度磷酸化或截断)通过CEBPB-ANP32A-INHAT通路抑制基因IST1的表达,导致IST1蛋白水平下降。IST1是内涵体分选复合物ESCRT-III的正向调节因子,其缺失阻碍ESCRT-III复合物(含CHMP2B、CHMP4B等组分)的形成,进而抑制自噬体与溶酶体的融合,引发自噬障碍。
病理性磷酸化:激酶(GSK-3β、CDK5)过度激活或磷酸酶(PP1、PP2A)失活,导致Tau异常磷酸化(如P-tau-S396),脱离微管并聚集,诱发突触功能障碍和神经元死亡。
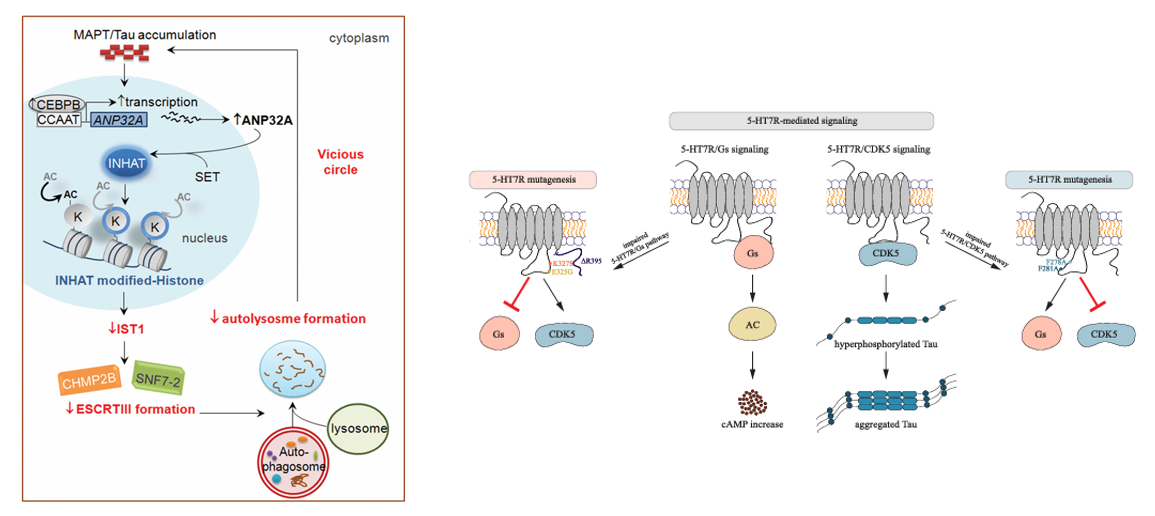
(数据来源左:Feng Q, et al. Autophagy. 2020;右:Ackmann J, et al. Cell Commun Signal. 2024)
MAPT与疾病
MAPT(微管相关tau蛋白)基因突变或功能异常是多种神经退行性疾病的核心病理机制,主要导致tau蛋白异常聚集形成神经元内包涵体,引发神经元功能障碍和死亡。
阿尔茨海默病(Alzheimer’s disease, AD):在阿尔茨海默病中,细胞外存在淀粉样蛋白-β和聚集Tau组成的老年斑。这些异常蛋白通过与表面受体互作,激活病理性Rho-GTPase信号通路。淀粉样蛋白-β暴露会高度激活Rho-GTPases(如Y42磷酸化)。其过度激活进而增强ROCK激酶活性。ROCK一方面磷酸化激活Src(Y416位点),进而激活促进Tau过度磷酸化的GSK-3β;另一方面抑制HDAC6活性(该酶促进Tau和微管蛋白乙酰化)。Tau的这些翻译后修饰最终导致其聚集。

(数据来源:Desale SE, et al. Mol Biomed. 2021)
家族性阿尔兹海默症(Familial Alzheimer's Disease , FAD):FAD相关PS1突变使γ-分泌酶活性升高,经APP-βCTF激活激酶(如GSK3),致Tau过度磷酸化聚集;细胞同步上调热休克蛋白(HSP90/70)、增强自噬(LC3-II、Lamp2参与),试图清除异常蛋白,但长期病理压力下,保护机制可能失效,最终推动AD病理进展。
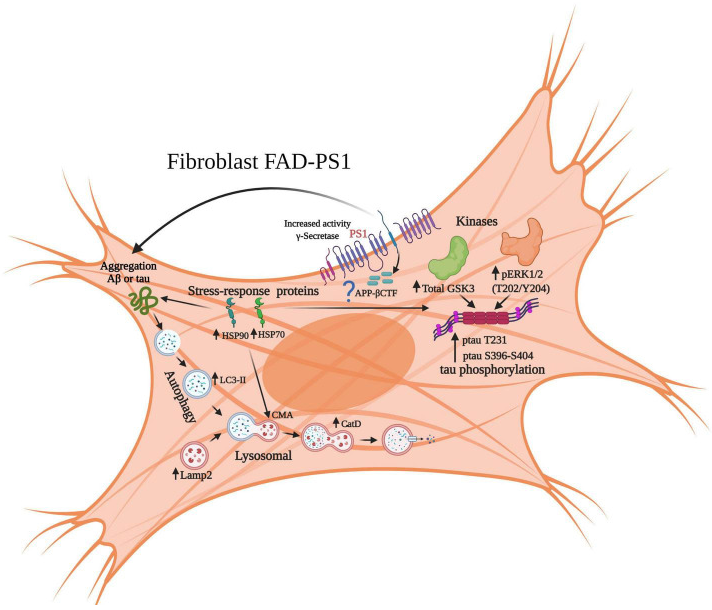
(数据来源:Lopez-Toledo G, et al. Front Aging Neurosci. 2022)
帕金森病(Parkinson's Disease,PD):PD患者脑内部分区域(如黑质纹状体)的Tau会过度磷酸化,导致其从微管上脱落,自身错误折叠并聚集为“神经原纤维缠结”。这种聚集直接破坏微管结构,阻断神经元内信号传导和物质运输。Tau还能与α-syn等病理事件协同,加速多巴胺能神经元死亡。
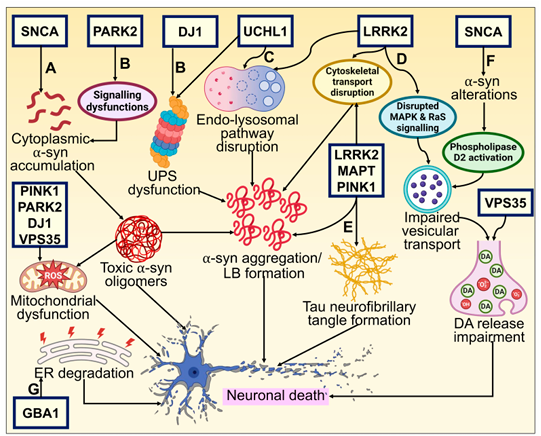
(数据来源:Ratan Y, et al. Biomolecules. 2024)
MAPT的靶向治疗
反义寡核苷酸可用于降低Tau蛋白表达。Tau蛋白聚集抑制剂包括姜黄素和亚甲蓝衍生物LMTX。像TPI-287和NAP这样的微管稳定剂,可用于弥补Tau蛋白正常微管稳定功能的丧失。利用自噬或蛋白酶体降解的调节剂,能够促进病理性Tau蛋白的清除。主动和被动免疫疗法借助抗体,在细胞内或细胞外靶向病理性Tau蛋白,促进其降解和清除。
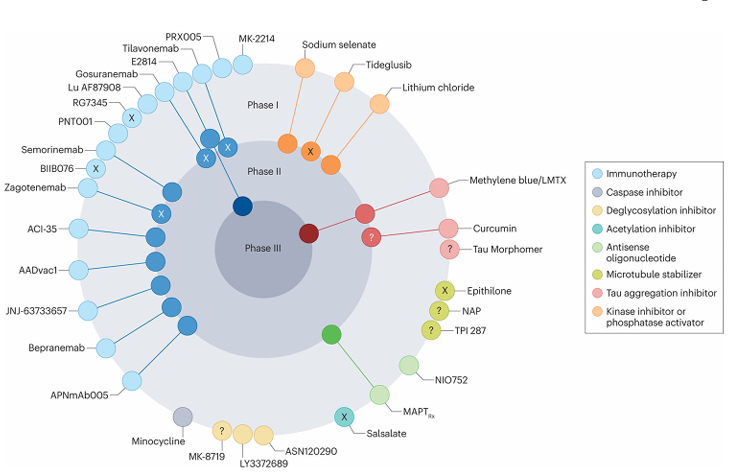
(数据来源:Congdon EE, et al. Nat Rev Neurol. 2023)
Etalanetug是由Eisai研发的一款靶向TAU的单克隆抗体药物。其主要的作用机制是作为TAU的抑制剂,用于治疗阿尔兹海默症和认知功能障碍。于2021年12月22日在首次批准3期临床试验。
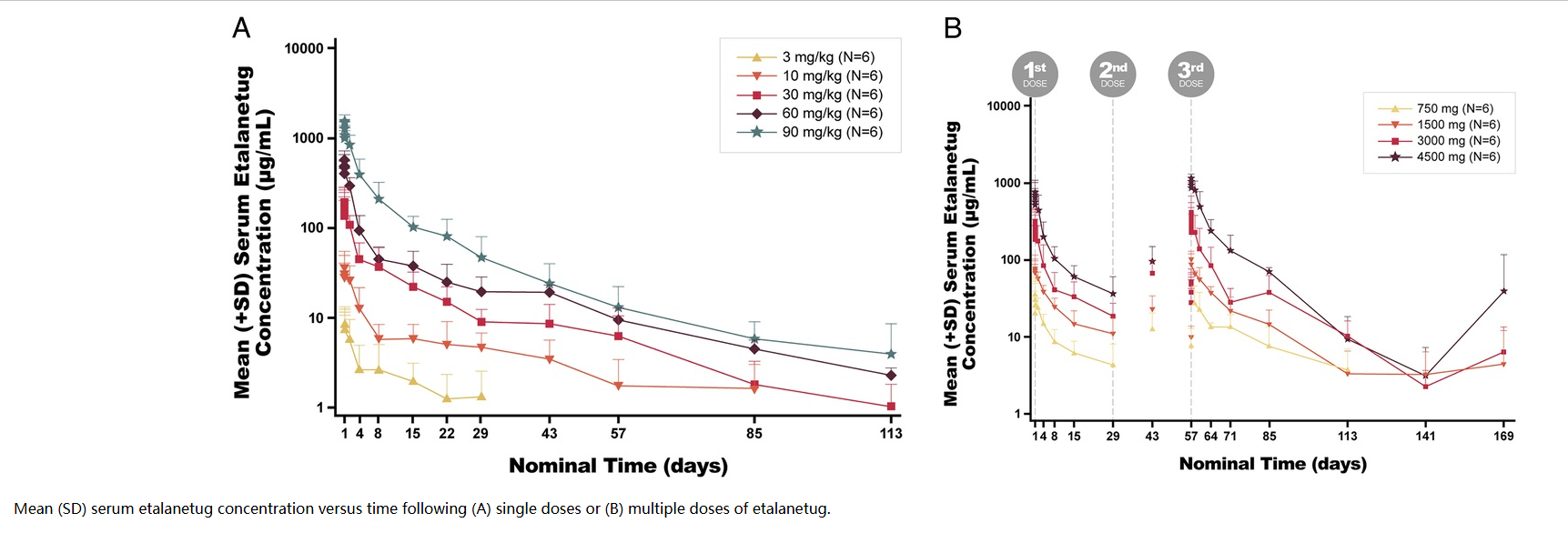
(数据来源:Rawal S, et al. Alzheimer Dis Assoc Disord. 2025)
MK-2214是由Merck研发的一款靶向TAU的单克隆抗体药物。其主要的作用机制是作为TAU的抑制剂,用于治疗阿尔兹海默症和认知功能障碍。于2025年7月16日首次批准2期临床试验。Tau抗体通过结合Tau聚集体、内吞后溶酶体降解、TRIM21介导蛋白酶体降解等方式,干预Tau蛋白异常聚集与清除,是阿尔茨海默病等Tau蛋白病免疫治疗策略之一。

(数据来源:Congdon EE, et al. Nat Rev Neurol. 2023)
VY-7523是由Voyager Therapeutics研发的一款靶向Tau单克隆抗体药物。其主要的作用机制作为TAU的抑制剂,用于治疗阿尔兹海默症和皮克病性痴呆及进行性核上性麻痹。于2025年3月3日首次批准2期临床试验。
PRX-005(BMS-986446)是由Prothena研发的一款靶向Tau的单克隆抗体药物。其主要的作用机制是作为Tau的调节剂,用于治疗阿尔兹海默症。于2024年3月20日首次批准2期临床试验。
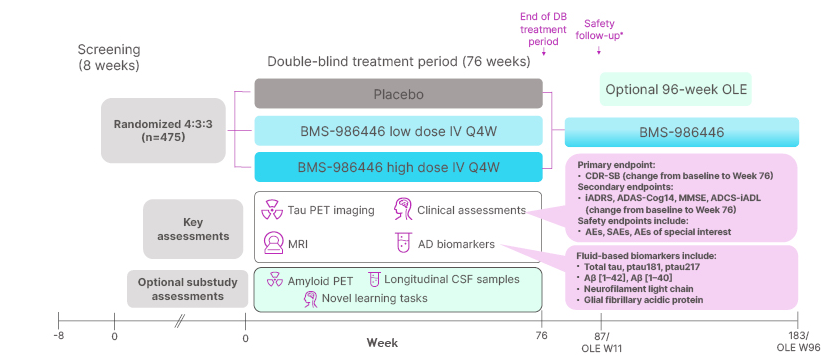
(数据来源:Christopher H, et al. The Journal of The Alzheimer 'S Association 2025)
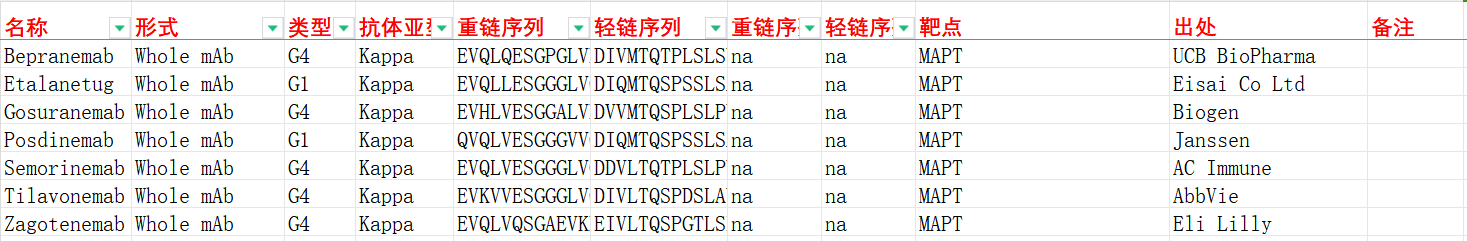
我们收集整理一批MAPT相关抗体序列信息。文档可关注公众号“迈思生物”,号内回复“ MAPT ”下载。