唾液酸结合免疫球蛋白样凝集素8(Sialic acid-binding Ig-like lectin 8,SIGLEC8),是一种跨膜蛋白,其主要功能是作为一种 抑制性受体,SIGLEC8的作用类似于免疫系统的“刹车装置”。它通过识别“自我”标志(唾液酸),防止这些细胞的过度活化和增殖,从而帮助限制炎症和过敏反应的强度与持续时间,避免对机体造成损伤。
SIGLEC8的表达分布
SIGLEC8特异性表达于血细胞,即嗜碱性粒细胞、肥大细胞和嗜酸性粒细胞。这三种细胞是过敏反应(如哮喘、特应性皮炎)和某些炎症性疾病中的关键效应细胞。
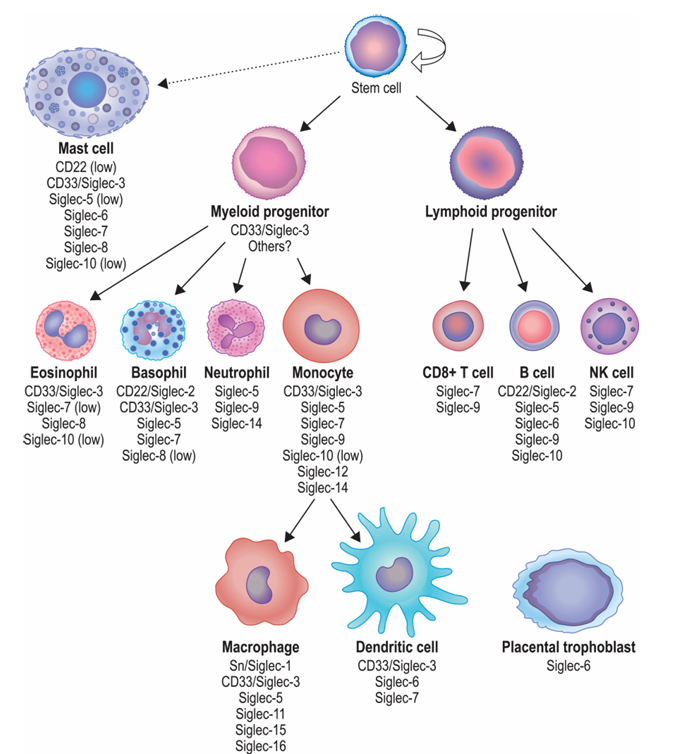
(数据来源:O'Sullivan JA, et al.J Leukoc Biol. 2020)
SIGLEC8的结构
SIGLEC8是由SIGLEC8基因编码的长度为499 aa,分子量约54 kDa的Ⅰ型跨膜蛋白,由胞内区,跨膜区和胞外区三个部分组成,并通过选择性剪接生成多种异构体(如长型SIGLEC8-b、短型SIGLEC8-a/c/d/f、可溶型SIGLEC8-e)。
胞外区(17-363 aa):a) N端V-set Ig样结构域:这是唾液酸结合位点 所在的核心结构域。它能够特异性识别并结合含有 唾液酸 的糖基配体。该结合具有特异性,SIGLEC8优先结合其配体 6'-磺基-唾液酸路易斯X。b)2个Ig样C2结构域:位于V-set结构域之后,主要起支撑和延伸的作用,使V-set结构域能够更灵活地接近细胞表面的糖配体。
跨膜区(364-384 aa):由一个α螺旋组成,其主要功能是将受体锚定在细胞膜上,并将胞外区的构象变化传递到胞内区。
胞质区(385-499 aa):这是其信号转导功能的关键所在。免疫受体酪氨酸抑制基序:这是SIGLEC8传递抑制性信号的核心。当ITIM中的酪氨酸被磷酸化后,它会招募并激活含有SH2结构域的蛋白酪氨酸磷酸酶,从而拮抗和抑制免疫细胞的激活信号,最终导致细胞功能的抑制。
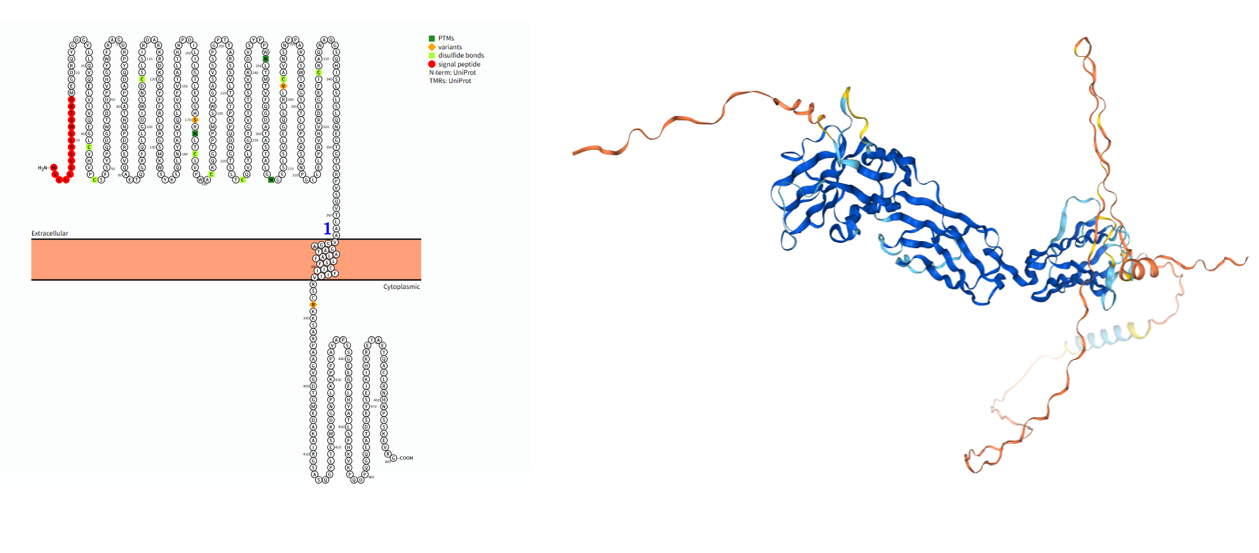
(数据来源:protter)
SIGLEC8的信号通路
SIGLEC8的信号通路是其 抑制性功能 的结构基础,核心在于其胞内段所携带的 免疫受体酪氨酸抑制基序(ITIM) 和 一个假定的ITIM-like基序。该通路在嗜酸性粒细胞和肥大细胞中略有不同,但核心机制相似。
a)在嗜酸性粒细胞中:抗SIGLEC8抗体先与嗜酸性粒细胞表面顺式连接的SIGLEC8结合形成载药抗体,引发肌动蛋白重排、激活酪氨酸激酶及PKC,继而经网格蛋白介导和脂筏介导的内吞作用进入细胞,在溶酶体中最终释放货物。
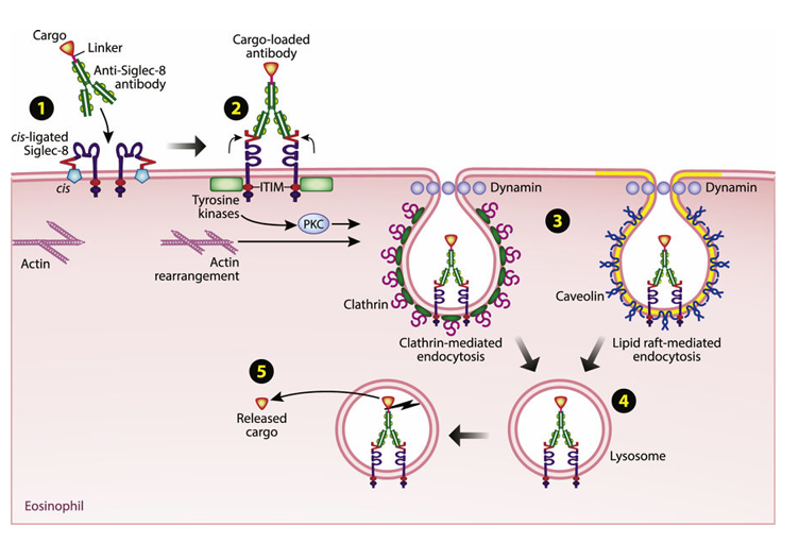
(数据来源:O'Sullivan JA, et al.J Allergy Clin Immunol. 2018)
b)在肥大细胞中:这条通路的激活更间接。一方面,JAK2可以磷酸化胰岛素受体底物(IRS)蛋白,使其招募并激活PI3K。另一方面,STAT3的基因转录产物也可能间接影响该通路。
SHP-1/2的主要作用是抑制FcεRI(高亲和力IgE受体)介导的激活信号。它们去磷酸化FcεRI信号通路中的关键组分(如Syk、LAT等),从而抑制钙离子内流,抑制NF-κB和MAPK等炎症通路的激活,最终强烈抑制肥大细胞的脱颗粒(释放组胺、类胰蛋白酶等)和炎症因子产生。
SIGLEC8与疾病
严重哮喘:特别是嗜酸性粒细胞型哮喘,气道中嗜酸性粒细胞浸润和脱颗粒,导致慢性炎症和支气管收缩。
Eosinophilic Esophagitis(嗜酸性粒细胞性食管炎):嗜酸性粒细胞在食管壁大量聚集,引起吞咽困难、食物嵌塞和反流等症状。
Alzheimer's disease(阿尔兹海默症)领域: SIGLEC-8作用体现为:
a)生理状态下:主要位于细胞内,通过调控小胶质细胞等活动维持神经元突触功能及神经组织稳态。
b)神经炎症状态下:则出现在细胞外,参与小胶质细胞和星形胶质细胞激活后的信号传导,并与β-淀粉样纤维等病理物质关联,影响神经炎症进程。
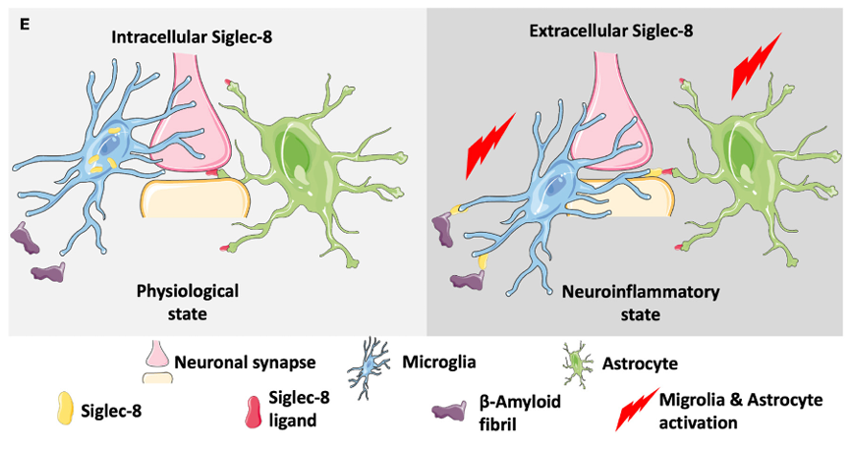
(数据来源:Dhar C et al. Front Cell Neurosci. 2023)
胃肠道领域:SIGLEC-8通过免疫调控与维持肠道稳态发挥功能。它表达于嗜酸性粒细胞等免疫细胞表面,通过识别配体调节细胞活性,例如抑制嗜酸性粒细胞释放ECP、MBP等介质,从而调节免疫反应强度,防止过度激活导致组织损伤。在肠道中,它参与维持屏障功能与免疫细胞平衡,通过调控免疫应答助力保持肠道正常生理状态,减少免疫紊乱引发的肠道功能异常及肠-脑互动相关共病。
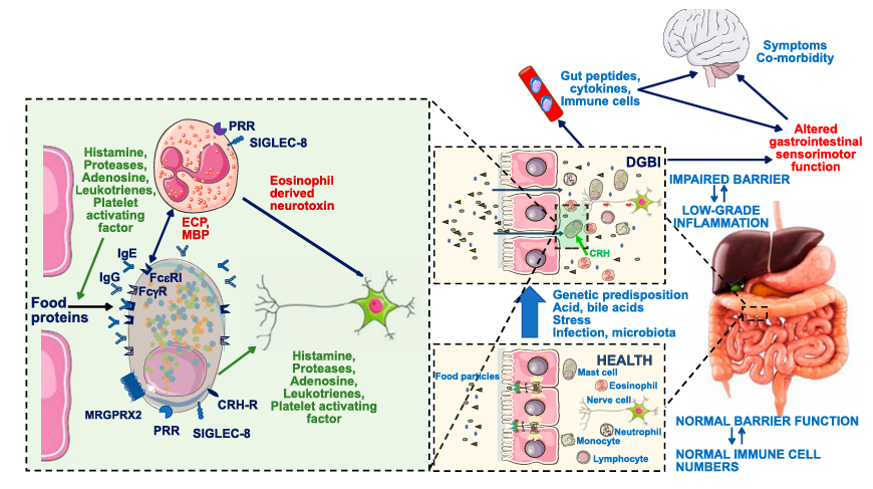
(数据来源:Van den Houte K et al. Am J Gastroenterol. 2022)
urticaria(荨麻疹) /Inflammatory and Allergic Diseases(炎症和过敏性疾病)领域:SIGLEC8作为抑制性受体。a)抑制信号传导:可阻止肥大细胞过度激活,避免其大量释放组胺(Histamine)、类胰蛋白酶(Tryptase)、白三烯(Leukotrienes)等炎症介质,进而减少因这些介质释放引发的支气管收缩、血管通透性增加等炎症反应。b)平衡免疫反应:有助于维持机体免疫稳态,防止因肥大细胞异常活化而导致的过敏或炎性疾病,在免疫调节中起到维持平衡的作用。
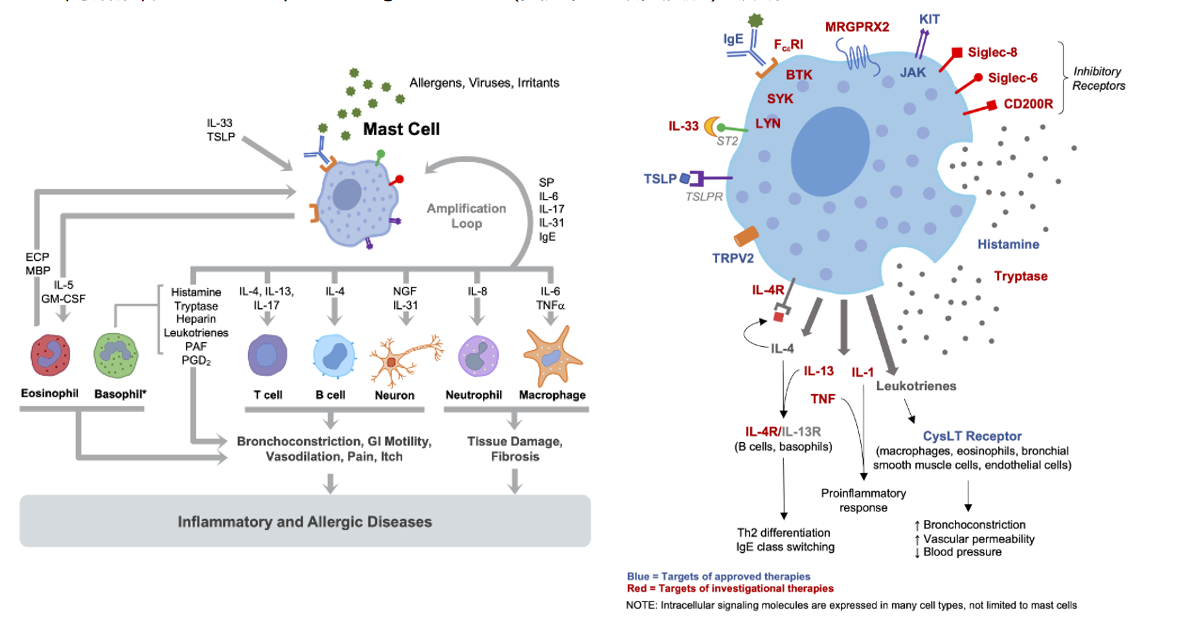
(数据来源:Metz M, et al.Allergy. 2024)
SIGLEC8的靶向治疗
在人(Human)与小鼠(Mouse)中,靶向Siglec-8和其功能同源分子Siglec-F的抗体所介导的细胞死亡机制存在显著差异。在人中,抗体结合Siglec-8后能直接通过多种内在途径诱导细胞死亡,包括依赖ROS、线粒体功能障碍及Caspase激活等,并伴有ADCC作用,其内吞方式为网格蛋白及脂筏/小窝蛋白依赖。而在小鼠中,抗体结合Siglec-F后不能直接引起强效的内在细胞死亡,其主要依赖ADCC/ADCP等效应机制清除细胞,内吞为网格蛋白依赖但发动蛋白非依赖方式,且需重复注射才能增强细胞死亡效果。
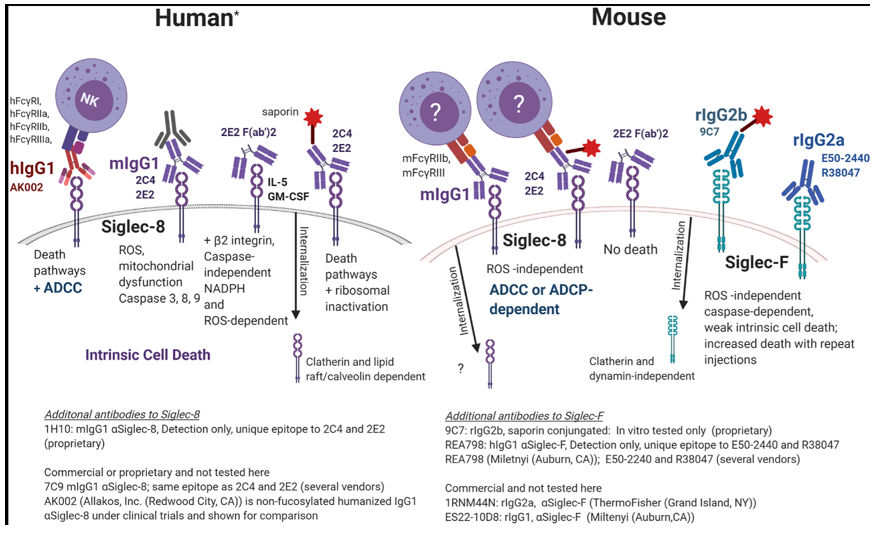
(数据来源:Dhar C et al. Front Cell Neurosci. 2023)
Antolimab是由Allakos联合研发的一款靶向SIGLEC8的单克隆抗体药物。其主要的作用机制是作为SIGLEC8的抑制剂,通过抑制Siglec-8受体功能,阻断其介导的免疫抑制信号通路,从而减少肥大细胞活化和炎症反应1;同时具有肥大细胞抑制作用,可降低组胺、前列腺素等炎症介质的释放,用于治疗慢性荨麻疹和嗜酸性粒细胞食管炎及髓性系统性肥大细胞增多症。于2020年6月18日批准3期临床试验。
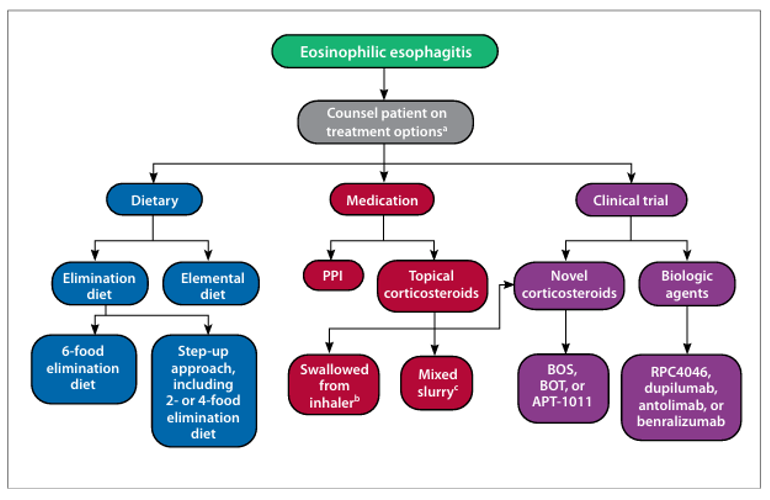
(数据来源:Beveridge C, et al. Gastroenterol Hepatol (N Y). 2020)
AK-001是由Allakos研发的一款靶向SIGLEC8的单克隆抗体药物。其主要的作用机制是作为SIGLEC8的抑制剂调节免疫细胞(如嗜酸性粒细胞、肥大细胞)的活性,抑制过度免疫反应,通过免疫调节作用改善过敏性疾病和慢性炎症相关病理过程,用于治疗耳鼻咽喉疾病、呼吸系统疾病、皮肤和肌肉骨骼疾病。于2016年4月1日批准2期临床试验,但目前没有进展。
我们收集整理一批SIGLEC8相关抗体序列信息。文档可关注公众号“迈思生物”,号内回复“ SIGLEC8 ”下载。
