服务支持
迈思生物承担了人源NAMPT的重组蛋白表达服务。

背景
钙化性主动脉瓣疾病(CAVD)已成为一种主要的年龄相关心血管流行病,影响超过12%的65岁以上人群,表现为从早期纤维钙化病变向重度主动脉瓣狭窄的进行性过渡。随着全球人口老龄化,CAVD是心血管疾病死亡的第三大原因。虽然CAVD的致病机制正在逐步阐明,但与年龄相关的主动脉瓣生物学改变仍不清楚。衰老研究的最新进展发现了共同的特征,包括细胞衰老、慢性炎症和线粒体功能障碍,这些特征驱动机体衰老和CAVD发病。
烟酰胺腺嘌呤二核苷酸(NAD)作为调控细胞生物能量学与信号转导的主要代谢调节因子,在衰老过程中会逐渐减少。在心脏组织中,超过85%的NAD生成高度依赖于补救途径的限速酶,烟酰胺磷酸核糖转移酶(NAMPT)。瓣膜钙化进展过程中NAMPT的时空动态变化,及其对瓣膜细胞命运决定的精确调控机制,仍有待系统性研究。

2026年3月17日华中科技大学同济医学院附属协和医院董念国团队在Eur Heart J上发表了一篇名为“Senescence-associated metabolic alterations aggravate calcific aortic valve disease”的研究成果。研究发现,衰老的主动脉瓣中代谢重配置的主要形式是抑制NAMPT介导的修复途径。在单细胞水平上,描绘了瓣膜内皮细胞(VECs)和巨噬细胞之间异质性的NAMPT表达模式,揭示了细胞间的相互作用,这种相互作用协调了钙化过程。此外,还发现巨噬细胞内在的NAMPT异质性在推动冠状动脉血管疾病(CAVD)进展方面具有双重功能,促进炎症激活和细胞外基质(ECM)重塑。这些发现表明,内皮细胞中NAMPT的缺乏是与年龄相关的CAVD的主要起始因素,在此过程中,招募的巨噬细胞通过炎症级联反应和胶原蛋白降解来放大疾病。
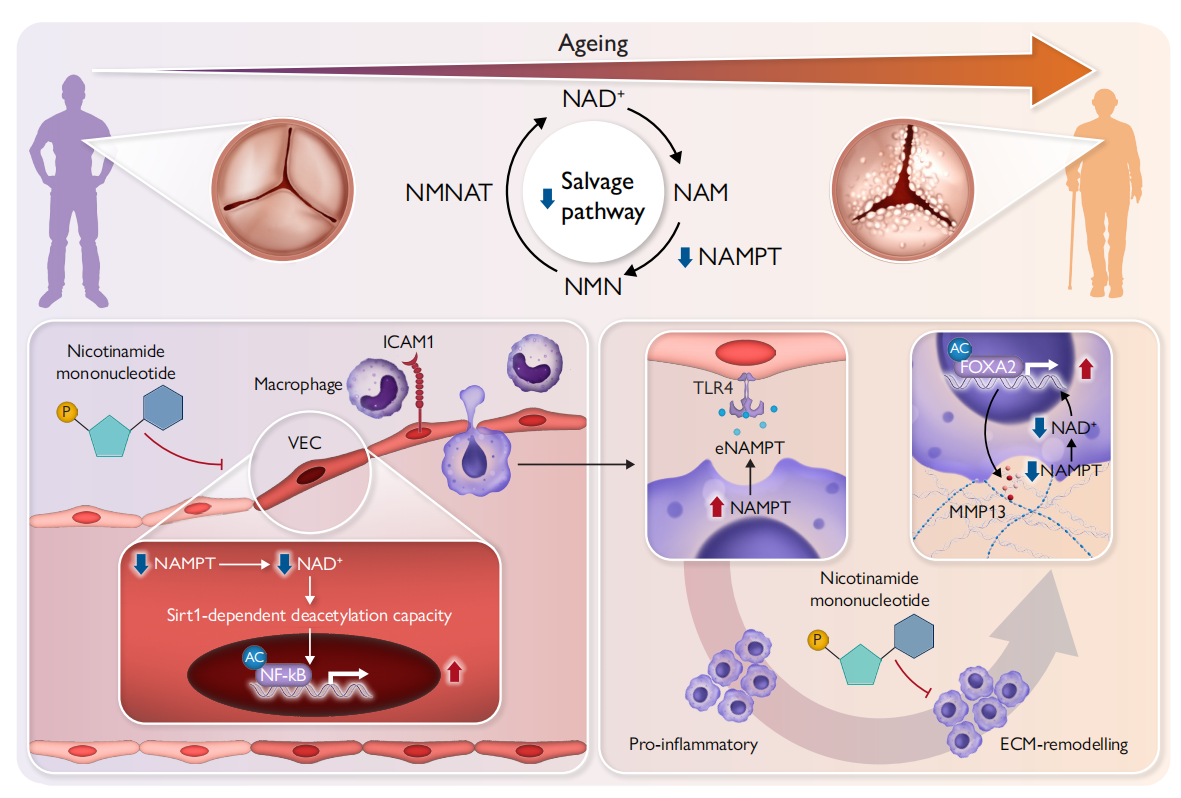
衰老的人主动脉瓣中NAMPT介导的NAD+补救途径显著下调
转录组分析显示,在衰老的人主动脉瓣中,NAD+合成关键酶NAMPT的表达下降最为显著,且这种下降与年龄强相关而非疾病严重程度。即使在无明显钙化的老年瓣膜中,NAD+水平降低和早期成骨信号激活也已出现,表明这是衰老相关的早期重塑标志。

NAMPT缺乏加重小鼠主动脉瓣钙化和心功能不全
杂合子NAMPT缺失小鼠在高脂饮食下比野生型更早出现主动脉瓣狭窄、瓣叶增厚及钙化,并伴随射血分数下降和心肌纤维化,说明NAMPT单倍剂量不足会加剧由年龄驱动的内在瓣膜重塑。清除衰老细胞的治疗在野生型小鼠中有效,但在NAMPT缺失小鼠中效果有限,这表明NAMPT缺乏会加剧衰老过程中纤维化-钙化轨迹的难治性。

单细胞测序揭示内皮细胞NAMPT下调驱动巨噬细胞招募
单细胞RNA测序发现,衰老瓣膜中瓣膜内皮细胞(VECs)的NAMPT表达下降最明显,而浸润的巨噬细胞中NAMPT表达反而上调。在老年人类主动脉瓣中,血管内皮细胞(VECs)与单核吞噬细胞之间的相互作用显著增强。这些发现表明衰老过程中内皮NAMPT表达下调与CXCL介导的内皮-巨噬细胞交互作用增强以及炎症性巨噬细胞募集过程密切相关。

NAMPT下调通过NF-κB乙酰化的升高驱动瓣膜内皮细胞的炎症
通过药物抑制NAMPT(FK866)以及基因敲除实验,均显著上调了VEC中ICAM1和VCAM1的表达,并显著抑制了SIRT1的去乙酰化酶活性。至关重要的是,SIRT1的缺失现象与这种炎症激活现象相似,其机制是通过增强NF-κB p65的乙酰化来实现的,这是一种促进核转移并增强促炎转录的翻译后修饰。综上,这些发现表明NAMPT下调通过损害SIRT1介导的去乙酰化作用驱动血管内皮细胞炎症反应,导致NF-κB活化水平升高。

早期补充NMN可减轻小鼠瓣膜炎症并延缓钙化进展
组织病理学分析确立了治疗窗口期:对单倍剂量不足小鼠和条件性敲除小鼠进行早期干预可减少瓣膜厚度并抑制钙化,而晚期干预则未产生显著获益。这些结果确立了NMN作为一种有效的早期干预策略来减缓CAVD进展。然而,它在已建立的钙化环境中的疗效似乎有限,证据主要限于分子水平的衰减,而不是明显的逆转,因此强调了对效应巨噬细胞动态变化特征的需要。

巨噬细胞中NAMPT的适应性上调与异质性
在转录组和蛋白质水平上,高NAMPT表达与促炎性巨噬细胞极化之间存在显著关联,NAMPT上调作为适应性反应,可支持促炎极化过程中的能量需求。

巨噬细胞来源的细胞外NAMPT可放大内皮炎症
NAMPT通过不同的细胞内形式(iNAMPT)和细胞外形式(eNAMPT)发挥作用,其中eNAMPT可作为炎症级联反应的强效放大器。从机制上讲,药理学抑制(TAK242)或内皮TLR4的基因敲除显著减弱了rhNAMPT诱导的NF-κB 信号。eNAMPT作为损伤相关分子模式(DAMP),通过与内皮细胞表面的TLR4受体结合,进一步放大内皮炎症,形成恶性循环。巨噬细胞来源的eNAMPT直接驱动VECs的炎症激活。

衰老巨噬细胞通过FOXA2乙酰化来驱动MMP13介导的瓣膜胶原重塑
衰老的BMDMs中NAD+的清除促进FOXA2乙酰化,从而增强MMP13的转录。这种级联反应最终导致ECM降解,最终导致瓣膜钙化。值得注意的是,补充NMN也代表了一种有希望的治疗策略来对抗这种病理进展。

小结
该研究揭示了随着衰老VECs中NAMPT水平降低,会损害NAM向NMN的转化,削弱SIRT1介导的p65去乙酰化作用,并激活NF-κB,从而增加ICAM1的表达以招募巨噬细胞。巨噬细胞来源的eNAMPT会激活内皮细胞TLR4,而与衰老相关的重塑巨噬细胞会诱导FOXA2-MMP13介导的基质破坏,加速钙化;补充NMN可能会打破这一循环。钙化性主动脉瓣疾病是由内皮NAD+缺乏所引发的,并且会因代谢各异的巨噬细胞而加剧。这种分隔式的NAD+循环将炎症衰老与基质灾难联系起来。通过烟酰胺单核苷酸进行早期NAD+补充以及针对NAMPT的干预措施值得在临床上进行评估,作为治疗钙化性主动脉瓣疾病的潜在疗法。
